Densidade de gases UFSE
2 participantes
Página 1 de 1
 Densidade de gases UFSE
Densidade de gases UFSE
(UFSE) Após análise, certo gás mostrou ter densidade de 1,04 g/L, medida a 1 atm e 30 graus celsius. A fórmula molecular desse gás é:
Dados: Volume molar de gás a 1 atm e 30 graus celsius= 25 L/mol, C=12 g/mol, H= 1g/mol.
a) CH
b) CH4
c) C2H2
d) C2H6
e) C6H6
Dados: Volume molar de gás a 1 atm e 30 graus celsius= 25 L/mol, C=12 g/mol, H= 1g/mol.
a) CH
b) CH4
c) C2H2
d) C2H6
e) C6H6
Última edição por euler.cruz_ em Ter 09 Nov 2021, 09:36, editado 1 vez(es)
euler.cruz_- Iniciante
- Mensagens : 7
Data de inscrição : 08/11/2021
Idade : 22
 Re: Densidade de gases UFSE
Re: Densidade de gases UFSE
Olá euler;
Relacionando a densidade do gás com seu volume molar, podemos determinar sua massa molar, logo:
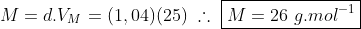
A única molécula que apresenta essa massa molecular é a do C2H2, veja:

Espero ter ajudado!
Relacionando a densidade do gás com seu volume molar, podemos determinar sua massa molar, logo:
A única molécula que apresenta essa massa molecular é a do C2H2, veja:
Espero ter ajudado!

qedpetrich- Monitor

- Mensagens : 2495
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
euler.cruz_ gosta desta mensagem
 Re: Densidade de gases UFSE
Re: Densidade de gases UFSE
Valeu mano, estava fazendo totalmente diferente com a formula da densidade de gases 
euler.cruz_- Iniciante
- Mensagens : 7
Data de inscrição : 08/11/2021
Idade : 22
qedpetrich gosta desta mensagem
 Re: Densidade de gases UFSE
Re: Densidade de gases UFSE
Pode ser feito sim, relacionando a definição de densidade com a Equação de Clapeyron, acredito que você conheça, não vou deduzir, somente aplicá-la, temos que:
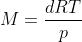
Possuímos todas as constantes, densidade, temperatura e pressão, dependemos somente de R, podemos determinar, utilizando a informação de volume molar, portanto:
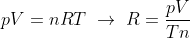
Sendo V.n⁻¹ = 25 L.mol⁻¹, logo:
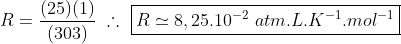
Substituindo:
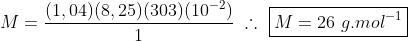
Mas perceba que fazendo desta forma é mais trabalhoso. Basta tomar que:
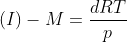
E por Clapeyron:
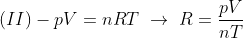
Substituindo (II) em (I):
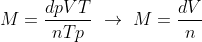
Mas como já explicado o volume molar é dado por V.n⁻¹, portanto:
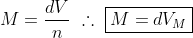
Que foi justamente a relação que utilizei.
Espero ter clareado sua mente!
Possuímos todas as constantes, densidade, temperatura e pressão, dependemos somente de R, podemos determinar, utilizando a informação de volume molar, portanto:
Sendo V.n⁻¹ = 25 L.mol⁻¹, logo:
Substituindo:
Mas perceba que fazendo desta forma é mais trabalhoso. Basta tomar que:
E por Clapeyron:
Substituindo (II) em (I):
Mas como já explicado o volume molar é dado por V.n⁻¹, portanto:
Que foi justamente a relação que utilizei.
Espero ter clareado sua mente!

qedpetrich- Monitor

- Mensagens : 2495
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
euler.cruz_ gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» Densidade dos Gases
» Densidade dos Gases
» densidade de gases
» Lei dos Gases ideais- Densidade
» Mistura gasosa e densidade dos gases.
» Densidade dos Gases
» densidade de gases
» Lei dos Gases ideais- Densidade
» Mistura gasosa e densidade dos gases.
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













