Solução
2 participantes
Página 1 de 1
 Solução
Solução
O carbonato de sódio, Na2CO3, é usado na absorção e no tratamento de gases de exaustão de usinas termoelétricas, alimentadas a carvão e a óleo. Uma amostra de 10,0g do produto impuro, utilizado na absorção dos gases, foi totalmente dissolvido em 600,0mL de solução de ácido clorídrico, HCl(aq), 2,0.10−1molL−1, e o excesso de ácido foi neutralizado com 250,0mL de hidróxido de sódio, NaOH, 1,0.10−1molL−1.
A análise das informações, referidas no texto, permite corretamente afirmar:
01) A massa de carbonato de sódio, na amostra, é, aproximadamente, 5,04g.
02) A quantidade de matéria de carbonato de sódio que reage é o dobro da de ácido clorídrico.
03) O teor de carbonato de sódio, em percentagem de massa, na amostra do produto impuro, é de 52,5%.
04) O excesso de ácido clorídrico, neutralizado por hidróxido de sódio, corresponde, aproximadamente, a 1,0g.
05) A quantidade de matéria de HCl(aq) que reage com todo o carbonato de sódio existente na amostra é 2,5.10^−2mol.
Gostaria da resposta de cada alternativa, grato
A análise das informações, referidas no texto, permite corretamente afirmar:
01) A massa de carbonato de sódio, na amostra, é, aproximadamente, 5,04g.
02) A quantidade de matéria de carbonato de sódio que reage é o dobro da de ácido clorídrico.
03) O teor de carbonato de sódio, em percentagem de massa, na amostra do produto impuro, é de 52,5%.
04) O excesso de ácido clorídrico, neutralizado por hidróxido de sódio, corresponde, aproximadamente, a 1,0g.
05) A quantidade de matéria de HCl(aq) que reage com todo o carbonato de sódio existente na amostra é 2,5.10^−2mol.
Gostaria da resposta de cada alternativa, grato
nudwu92- Recebeu o sabre de luz

- Mensagens : 195
Data de inscrição : 15/05/2017
Idade : 26
Localização : salvadorr
 Re: Solução
Re: Solução
I) Cálculo do número de mols de HCl que reagiram com o NaOH:
HCl + NaOH ---> NaCl + H2O (reação)
Dado que a relação é 1:1, temos que:
1x10^-1 mol ------ 1000ml
x -------250ml
x=2,5 x 10^-2 mol de HCl que sobraram para reagir com NaOH.
II) Cálculo do n de mols total de HCl:
2X10^-1 mol ----- 1000 ml
y --- 600 ml
y = 12 x 10^-2 mols
III) Cálculo do n de mols que reagiram com Na2CO3:
(12 - 2,5) X 10^-2 = 9,5 X 10^-2 mols
IV) Reação do HCl com o Na2CO3:
Na2CO3 + 2HCl -> H2CO3 + 2NaCL
Dada que a relação é 2:1, temos que:
1 mol ----- 106 g
9,5 x 10^-2 / 2 ---- z
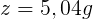
Analisando as alternativas:
01) A massa de carbonato de sódio, na amostra, é, aproximadamente, 5,04g. (CORRETA)
02) A quantidade de matéria de carbonato de sódio que reage é o dobro da de ácido clorídrico. (NÃO, É JUSTAMENTE O INVERSO)
03) O teor de carbonato de sódio, em percentagem de massa, na amostra do produto impuro, é de 52,5%. ( NA VERDADE, É 50,40%)
04) O excesso de ácido clorídrico, neutralizado por hidróxido de sódio, corresponde, aproximadamente, a 1,0g. ( O RESULTADO É 0,9125g)
05) A quantidade de matéria de HCl(aq) que reage com todo o carbonato de sódio existente na amostra é 2,5.10^−2mol. ( ESSA É A QUANTIDADE QUE REAGE COM O NaOH).
Abç!
HCl + NaOH ---> NaCl + H2O (reação)
Dado que a relação é 1:1, temos que:
1x10^-1 mol ------ 1000ml
x -------250ml
x=2,5 x 10^-2 mol de HCl que sobraram para reagir com NaOH.
II) Cálculo do n de mols total de HCl:
2X10^-1 mol ----- 1000 ml
y --- 600 ml
y = 12 x 10^-2 mols
III) Cálculo do n de mols que reagiram com Na2CO3:
(12 - 2,5) X 10^-2 = 9,5 X 10^-2 mols
IV) Reação do HCl com o Na2CO3:
Na2CO3 + 2HCl -> H2CO3 + 2NaCL
Dada que a relação é 2:1, temos que:
1 mol ----- 106 g
9,5 x 10^-2 / 2 ---- z
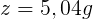
Analisando as alternativas:
01) A massa de carbonato de sódio, na amostra, é, aproximadamente, 5,04g. (CORRETA)
02) A quantidade de matéria de carbonato de sódio que reage é o dobro da de ácido clorídrico. (NÃO, É JUSTAMENTE O INVERSO)
03) O teor de carbonato de sódio, em percentagem de massa, na amostra do produto impuro, é de 52,5%. ( NA VERDADE, É 50,40%)
04) O excesso de ácido clorídrico, neutralizado por hidróxido de sódio, corresponde, aproximadamente, a 1,0g. ( O RESULTADO É 0,9125g)
05) A quantidade de matéria de HCl(aq) que reage com todo o carbonato de sódio existente na amostra é 2,5.10^−2mol. ( ESSA É A QUANTIDADE QUE REAGE COM O NaOH).
Abç!
____________________________________________
"Copiar para criar, criar para competir e competir para vencer". Takeo Fukuda

Davi Paes Leme- Elite Jedi

- Mensagens : 209
Data de inscrição : 22/04/2016
Idade : 28
Localização : Rio de Janeiro
 Re: Solução
Re: Solução
Davi, muito obrigado! 
nudwu92- Recebeu o sabre de luz

- Mensagens : 195
Data de inscrição : 15/05/2017
Idade : 26
Localização : salvadorr
 Tópicos semelhantes
Tópicos semelhantes» solução
» Fuvest - dissolução de uma solução aquosa ácida através de solução aquosa básica
» PH - solução
» Solução
» Solução
» Fuvest - dissolução de uma solução aquosa ácida através de solução aquosa básica
» PH - solução
» Solução
» Solução
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













