Cinética química
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Cinética química
Cinética química
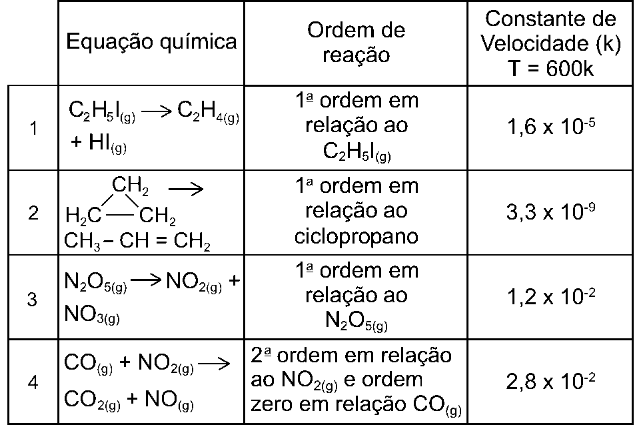
No quadro a seguir, encontram-se equações químicas, que representam reações realizadas em idênticas condições de temperatura e pressão; suas respectivas ordens de reação em relação aos reagentes; e as constantes de velocidade, obtidas experimentalmente. Pela análise do quadro, conclui-se que, quando a concentração molar dos reagentes é de 0,1 mol/L, a ordem crescente das velocidades das reações é
a)
b)
c)
d)
e)
Não consigo entender como V4 < V3

a)

b)

c)

d)

e)

Não consigo entender como V4 < V3
- Gabarito:
- D
vivixp123- Recebeu o sabre de luz

- Mensagens : 133
Data de inscrição : 21/05/2013
Idade : 27
Localização : brasil
 Re: Cinética química
Re: Cinética química
Bom dia,
Vamos calcularV_4 e V_3 pela fórmula de Guldeberg-Waage:
Para 4:
V_4=K[CO]^0[NO_2]^2=2,8\times10^{-2}\times(0,1)^2
V_4 = 2,28\times10^{-4}
Note que a ordem do reagente foi colocada como expoente na fórmula.
Para 3:
V_3=k[N_2O_5]=1,2\times10^{-2}\times0,1
V_3=1,2\times10^{-3}
E daí tiramos queV_4 < V_3
Entendeu o procedimento?
Vamos calcular
Para 4:
Note que a ordem do reagente foi colocada como expoente na fórmula.
Para 3:
E daí tiramos que
Entendeu o procedimento?
Última edição por GFMCarvalho em Qua 06 Jul 2016, 09:14, editado 1 vez(es) (Motivo da edição : Expoente incorreto para [CO])

GFMCarvalho- Jedi

- Mensagens : 232
Data de inscrição : 03/10/2015
Idade : 24
Localização : Itajubá, Minas Gerais, Brasil
 Re: Cinética química
Re: Cinética química
Sim, muito obrigado
vivixp123- Recebeu o sabre de luz

- Mensagens : 133
Data de inscrição : 21/05/2013
Idade : 27
Localização : brasil
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













