IME 1999
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 IME 1999
IME 1999
Considerando que 100% do calor liberado na combustão do metano sejam utilizados para converter 100 Kg de água a 10o C em vapor a 100oC. calcule o volume do metano consumido, medido nas CNTP, supondo que ele se comporte como um gás ideal.
Dados Constante universal dos gases perfeitos R= 0,082 atm.L/mol.K
Calor latente de vaporização da água = 2260 J/g
Calor específico da água = 4,2 J/g.oC
Calor de combustão do metano = 890 KJ/mol
Alguém sabe resolver essa?
jjbr4603- Iniciante
- Mensagens : 25
Data de inscrição : 11/12/2021
 Re: IME 1999
Re: IME 1999
Olá;
Calculando a quantidade de energia (calor) necessária para transformar 100 kg de água em vapor:

Calculando quantos mols de metano, a partir de sua combustão:
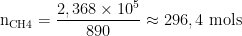
Por fim, calculando o volume nas condições normais de pressão e temperatura do gás metano:
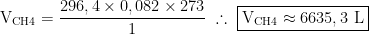
Penso ser isso. Você possui o gabarito?
Calculando a quantidade de energia (calor) necessária para transformar 100 kg de água em vapor:
Calculando quantos mols de metano, a partir de sua combustão:
Por fim, calculando o volume nas condições normais de pressão e temperatura do gás metano:
Penso ser isso. Você possui o gabarito?
____________________________________________
Dê tempo ao
Lateralus Φ

qedpetrich- Monitor

- Mensagens : 2498
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












