Questão de massa molar de compostos orgânicos
2 participantes
PiR2 :: Química :: Química Orgânica
Página 1 de 1
 Questão de massa molar de compostos orgânicos
Questão de massa molar de compostos orgânicos
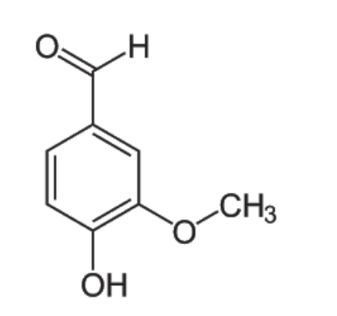
Como poderia resolver essa questão?
https://ibb.co/7Y29jMG
Última edição por iuryramos990_ em Sex 20 Nov 2020, 23:04, editado 1 vez(es)
iuryramos990_- Iniciante
- Mensagens : 13
Data de inscrição : 29/04/2020
 Re: Questão de massa molar de compostos orgânicos
Re: Questão de massa molar de compostos orgânicos
O enunciado fala que podemos perceber a Vanilina a partir de 2x10¨-13 em um litro. Isso é a Molaridade. Ou seja, eu tenho
2x10¨-13 mol em 1 L de ar. Basta fazer regra de três para descobrir quantos mols teremos em 80000 litros de ar na festa.
2x10¨-13 mol ----- 1 L
x mol --------- 80000L
Achando a quantidade de mol dentro desse volume, usaremos a fórmula do mol--> n=m/MM , onde "n" é mol, "m" é massa em gramas e "MM" massa molar.
Temos o n, agora ache o MM pela imagem contando os carbonos, hidrogênios escondidos e o oxigênio. Teremos C8H8O3
https://prnt.sc/vli4fe
"Dado: Massas molares (g/mol): H = 1; C= 12; O = 16." --> multiplique esses dados pela a quantidade de átomos existentes--> 12. 8 + 1.8+ 16.3 = 158 g/mol.
Agora substitui na fórmula n=m/MM, e ache a massa em gramas.
Qualquer dúvida só falar!
2x10¨-13 mol em 1 L de ar. Basta fazer regra de três para descobrir quantos mols teremos em 80000 litros de ar na festa.
2x10¨-13 mol ----- 1 L
x mol --------- 80000L
Achando a quantidade de mol dentro desse volume, usaremos a fórmula do mol--> n=m/MM , onde "n" é mol, "m" é massa em gramas e "MM" massa molar.
Temos o n, agora ache o MM pela imagem contando os carbonos, hidrogênios escondidos e o oxigênio. Teremos C8H8O3
https://prnt.sc/vli4fe
"Dado: Massas molares (g/mol): H = 1; C= 12; O = 16." --> multiplique esses dados pela a quantidade de átomos existentes--> 12. 8 + 1.8+ 16.3 = 158 g/mol.
Agora substitui na fórmula n=m/MM, e ache a massa em gramas.
Qualquer dúvida só falar!

Ceruko- Estrela Dourada

- Mensagens : 1326
Data de inscrição : 01/07/2020
Idade : 23
Localização : Ribeirão Preto
 Re: Questão de massa molar de compostos orgânicos
Re: Questão de massa molar de compostos orgânicos
O cálculo final seria: 0,000000016 = m/158 ?Ceruko escreveu:O enunciado fala que podemos perceber a Vanilina a partir de 2x10¨-13 em um litro. Isso é a Molaridade. Ou seja, eu tenho
2x10¨-13 mol em 1 L de ar. Basta fazer regra de três para descobrir quantos mols teremos em 80000 litros de ar na festa.
2x10¨-13 mol ----- 1 L
x mol --------- 80000L
Achando a quantidade de mol dentro desse volume, usaremos a fórmula do mol--> n=m/MM , onde "n" é mol, "m" é massa em gramas e "MM" massa molar.
Temos o n, agora ache o MM pela imagem contando os carbonos, hidrogênios escondidos e o oxigênio. Teremos C8H8O3
https://prnt.sc/vli4fe
"Dado: Massas molares (g/mol): H = 1; C= 12; O = 16." --> multiplique esses dados pela a quantidade de átomos existentes--> 12. 8 + 1.8+ 16.3 = 158 g/mol.
Agora substitui na fórmula n=m/MM, e ache a massa em gramas.
Qualquer dúvida só falar!
iuryramos990_- Iniciante
- Mensagens : 13
Data de inscrição : 29/04/2020
 Re: Questão de massa molar de compostos orgânicos
Re: Questão de massa molar de compostos orgânicos
Isso, 1,6x10^-8 =m/158

Ceruko- Estrela Dourada

- Mensagens : 1326
Data de inscrição : 01/07/2020
Idade : 23
Localização : Ribeirão Preto
 Tópicos semelhantes
Tópicos semelhantes» Questão UPE - Propriedade dos Compostos Orgânicos
» Questão sobre compostos orgânicos isômeros
» Questão massa molar e hidrocarbonetos
» FGV-SP Compostos orgânicos
» Compostos orgânicos
» Questão sobre compostos orgânicos isômeros
» Questão massa molar e hidrocarbonetos
» FGV-SP Compostos orgânicos
» Compostos orgânicos
PiR2 :: Química :: Química Orgânica
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












