Eletrólise
2 participantes
Página 1 de 1
 Eletrólise
Eletrólise
A figura abaixo representa um processo eletroquímico de uma solução aquosa de ácido sulfúrico, utilizando-se eletrodos inertes de platina. Responda às questões relacionadas a esse processo.
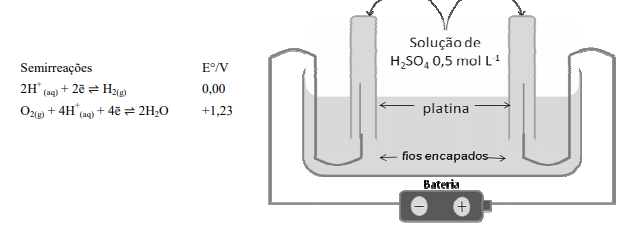
Quais as semirreações que ocorrem no anodo e no catodo?
Alguém sabe me explicar o porque de, no anodo, não termos a reação de oxidação do íon OH- e sim da água? Obrigada

Quais as semirreações que ocorrem no anodo e no catodo?
- Spoiler:
- Ânodo 2H2O ⇌ O2(g) + 4H+ (aq) + 4ē
Cátodo 2H+ (aq) + 2ē ⇌ H2(g)
Alguém sabe me explicar o porque de, no anodo, não termos a reação de oxidação do íon OH- e sim da água? Obrigada
brunamarc- Recebeu o sabre de luz

- Mensagens : 197
Data de inscrição : 09/10/2019
Idade : 24
Localização : Rio de Janeiro, RJ. Brasil.
 Re: Eletrólise
Re: Eletrólise
Olá, brunamarc
"Alguém sabe me explicar o porque de, no anodo, não termos a reação de oxidação do íon OH- e sim da água?"
Pois o meio é ácido, basicamente. Então se usa a reação de oxidação da água.
Uma dica bastante útil: use a descarga do H+ somente quando o meio estiver ácido e, a do OH-, quando o meio estiver básico. Caso contrário, use a descarga da água.
"Alguém sabe me explicar o porque de, no anodo, não termos a reação de oxidação do íon OH- e sim da água?"
Pois o meio é ácido, basicamente. Então se usa a reação de oxidação da água.
Uma dica bastante útil: use a descarga do H+ somente quando o meio estiver ácido e, a do OH-, quando o meio estiver básico. Caso contrário, use a descarga da água.
____________________________________________
Cha-la head-cha-la

Vitor Ahcor- Monitor

- Mensagens : 768
Data de inscrição : 21/12/2018
Idade : 24
Localização : São José dos Campos
brunamarc gosta desta mensagem
 Re: Eletrólise
Re: Eletrólise
Muito obrigada!! 
brunamarc- Recebeu o sabre de luz

- Mensagens : 197
Data de inscrição : 09/10/2019
Idade : 24
Localização : Rio de Janeiro, RJ. Brasil.
Vitor Ahcor gosta desta mensagem
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













