Unicamp 2000 - Constante de equilíbrio
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Unicamp 2000 - Constante de equilíbrio
Unicamp 2000 - Constante de equilíbrio
No tratamento da água, a fase seguinte à de separação é sua desinfecção. Um agente desinfetante muito
usado é o cloro gasoso que é adicionado diretamente à água. Os equilíbrios químicos seguintes estão
envolvidos na dissolução desse gás:
Cl2(aq) + H2O(aq) = HClO(aq) + H+(aq) + Cl-(aq) (I)
HClO(aq) = ClO-(aq) + H+(aq) (II)
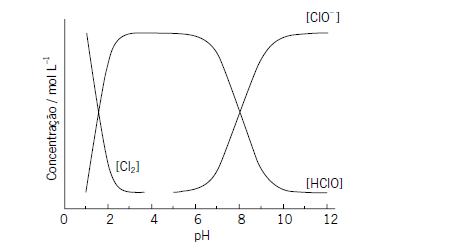
c) Calcule o valor da constante de equilíbrio referente à equação II.
Resolução da banca: no pH = 8, [H+] = 10–8
[ClO– ] = [HClO], Kc = 10-8
Minha resolução:
I) Do equilíbrio da reação I ---> pH=2 ---> [H+]=[HClO]=10-2 (concentração do HClO no equilíbrio da reação II)
II) Do equilíbrio da reação II pedida ---> pH=5 ---> [H+]=[ClO-]=10-5
III) Kc=10-10/10-2=10-8
Minha dúvida é: por que a banca escolheu um ponto fora do equilíbrio pra calcular a constante de equilíbrio? Kc tem algo a ver com o momento em que as concentrações se igualam?
usado é o cloro gasoso que é adicionado diretamente à água. Os equilíbrios químicos seguintes estão
envolvidos na dissolução desse gás:
Cl2(aq) + H2O(aq) = HClO(aq) + H+(aq) + Cl-(aq) (I)
HClO(aq) = ClO-(aq) + H+(aq) (II)

c) Calcule o valor da constante de equilíbrio referente à equação II.
Resolução da banca: no pH = 8, [H+] = 10–8
[ClO– ] = [HClO], Kc = 10-8
Minha resolução:
I) Do equilíbrio da reação I ---> pH=2 ---> [H+]=[HClO]=10-2 (concentração do HClO no equilíbrio da reação II)
II) Do equilíbrio da reação II pedida ---> pH=5 ---> [H+]=[ClO-]=10-5
III) Kc=10-10/10-2=10-8
Minha dúvida é: por que a banca escolheu um ponto fora do equilíbrio pra calcular a constante de equilíbrio? Kc tem algo a ver com o momento em que as concentrações se igualam?

Purcell- Iniciante
- Mensagens : 43
Data de inscrição : 29/04/2020
 Re: Unicamp 2000 - Constante de equilíbrio
Re: Unicamp 2000 - Constante de equilíbrio
Para achar a constante rápido pelo gráfico alfa de um ácido, você usa um resultado da equação de Henderson:
[latex]pH=pKa+log\left (\frac{Base\, Conjugada}{Acido} \right )[/latex]
Veja, se eu pegar o ponto que tem a mesma concentração de base conjugada e ácido, o pH correspondente é igual ao pKa do ácido sendo analisado, porque o log( [] / [] ) = log(1) = 0 ... pH = pKa
[latex]pH=pKa+log\left (\frac{Base\, Conjugada}{Acido} \right )[/latex]
Veja, se eu pegar o ponto que tem a mesma concentração de base conjugada e ácido, o pH correspondente é igual ao pKa do ácido sendo analisado, porque o log( [] / [] ) = log(1) = 0 ... pH = pKa

renan2014- Jedi

- Mensagens : 211
Data de inscrição : 04/07/2015
Localização : Rio de Janeiro
 Re: Unicamp 2000 - Constante de equilíbrio
Re: Unicamp 2000 - Constante de equilíbrio
Obrigado, renan2014 

Purcell- Iniciante
- Mensagens : 43
Data de inscrição : 29/04/2020
 Tópicos semelhantes
Tópicos semelhantes» UNICAMP - Constante de Equilíbrio
» (UNICAMP-2000) - dois números
» IME 2000 - Equilíbrio
» Constante de equilíbrio
» ITA - Constante de Equilíbrio
» (UNICAMP-2000) - dois números
» IME 2000 - Equilíbrio
» Constante de equilíbrio
» ITA - Constante de Equilíbrio
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













