Estequiometria VI
2 participantes
Página 1 de 2
Página 1 de 2 • 1, 2 
 Estequiometria VI
Estequiometria VI
Tem-se uma amostra impura de clorato de potássio pesando 3,00 g. Aquece-se a amostra em presença de um catalisador, MnO2, até massa constante; o resíduo obtido pesa 1,52 g. Este resíduo é dissolvido em água e o catalisador é retirado por filtração. A solução resultante é trata com excesso de nitrato de prata. Obtém-se um precipitado que após ter sido lavado e secado pesa 2,87 g. Qual a massa de clorato de potássio na amostra? Qual a massa do catalisador?
Eu encontrei o 2,45 g mas não estou conseguindo encontrar 0,03... Pensei que se 2,45 g é clorato, 0,55 g é impureza. Se 1,52 g é impureza + catalisador, a massa do catalisador deveria ser 0,97 g. Agradeço se apontarem o erro.
- resposta:
- 2,45 g e 0,03 g
Eu encontrei o 2,45 g mas não estou conseguindo encontrar 0,03... Pensei que se 2,45 g é clorato, 0,55 g é impureza. Se 1,52 g é impureza + catalisador, a massa do catalisador deveria ser 0,97 g. Agradeço se apontarem o erro.

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 11/03/2013
Localização : São Paulo
 Re: Estequiometria VI
Re: Estequiometria VI
Reação de calcinação do clorato de potássio:
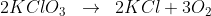
O oxigênio vai embora.. o catalisador permanece junto com o KCl , logo o resíduo a que ele se refere é a soma da massa do catalisador(x) com a do KCl: 1,52 = m(KCl) + x --> m(KCl) = 1,52 - x
Agora a reação do KCl com o AgNO3: (AgCl --> precipitado)
\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;&space;2,87\;&space;g\\\\&space;143,5(1,52&space;-&space;x)&space;=&space;74,5&space;\cdot&space;2,87&space;\;\;&space;\rightarrow&space;\;\;&space;\boxed{x&space;=&space;0,03\;&space;g})
Retomando a primeira reação e sabendo que a massa de KCl é de 1,49 g :
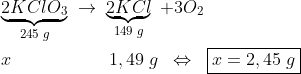
O oxigênio vai embora.. o catalisador permanece junto com o KCl , logo o resíduo a que ele se refere é a soma da massa do catalisador(x) com a do KCl: 1,52 = m(KCl) + x --> m(KCl) = 1,52 - x
Agora a reação do KCl com o AgNO3: (AgCl --> precipitado)
Retomando a primeira reação e sabendo que a massa de KCl é de 1,49 g :
____________________________________________
Thálisson.

Thálisson C- Monitor

- Mensagens : 3020
Data de inscrição : 19/02/2014
Idade : 27
Localização : Gurupi -TO
 Re: Estequiometria VI
Re: Estequiometria VI
1) Todo aquecimento pode ser chamado de calcinação?
2) No livro do Feltre lembro de ter lido que o catalisador nunca participa da reação, apenas a acelera. Esse problema é um cas especial, apenas?
3) Como 1,52 g é m(KCl) + x? E as impurezas não estão sendo incluídas na massa? Estou confuso quanto a isso.
Obrigado...
2) No livro do Feltre lembro de ter lido que o catalisador nunca participa da reação, apenas a acelera. Esse problema é um cas especial, apenas?
3) Como 1,52 g é m(KCl) + x? E as impurezas não estão sendo incluídas na massa? Estou confuso quanto a isso.
Obrigado...

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 11/03/2013
Localização : São Paulo
 Re: Estequiometria VI
Re: Estequiometria VI
Boas perguntas Ashitaka,
1) Reação de calcinação é aquela em que ocorre uma decomposição por aquecimento e geralmente liberando produtos gasosos. Por isso chamei ela assim. A reação mais conhecida é a de decomposição do carbonato de cálcio:
CaCO3 -----> CaO + CO2 (geralmente elas também formam óxidos)
Não estou completamente certo se essa reação do clorato pode ser de fato chamada assim, mas é um modelo bastante semelhante.
2) O catalisador nunca participa de reações químicas mesmo, se participar, deixa de ser catalisador. Por isso, um catalisador entra como reagente com uma massa y e sai nos produtos com a mesma massa y, sem ser consumido..
3) Eu nem havia pensado nas impurezas quando fiz o exercício, mas de fato elas existem mesmo, porém, acho que elas não podem ser chamadas de resíduo obtido, além do mais, exercício sugere que esse resíduo seja o sal (dissolvido em água) e o catalisador (que foi filtrado).
1) Reação de calcinação é aquela em que ocorre uma decomposição por aquecimento e geralmente liberando produtos gasosos. Por isso chamei ela assim. A reação mais conhecida é a de decomposição do carbonato de cálcio:
CaCO3 -----> CaO + CO2 (geralmente elas também formam óxidos)
Não estou completamente certo se essa reação do clorato pode ser de fato chamada assim, mas é um modelo bastante semelhante.
2) O catalisador nunca participa de reações químicas mesmo, se participar, deixa de ser catalisador. Por isso, um catalisador entra como reagente com uma massa y e sai nos produtos com a mesma massa y, sem ser consumido..
3) Eu nem havia pensado nas impurezas quando fiz o exercício, mas de fato elas existem mesmo, porém, acho que elas não podem ser chamadas de resíduo obtido, além do mais, exercício sugere que esse resíduo seja o sal (dissolvido em água) e o catalisador (que foi filtrado).
____________________________________________
Thálisson.

Thálisson C- Monitor

- Mensagens : 3020
Data de inscrição : 19/02/2014
Idade : 27
Localização : Gurupi -TO
 Re: Estequiometria VI
Re: Estequiometria VI
Que exercício estranho... um catalisador que reage e uma impureza que não faz diferença para resolver. 
Obrigado, Thálisson.
Obrigado, Thálisson.

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 11/03/2013
Localização : São Paulo
 Re: Estequiometria VI
Re: Estequiometria VI
Não Ashitaka, o catalisador não reagiu, ele apenas participou como acelerador da reação, tanto que eu nem coloquei MnO2 nas reações que apresentei.
E na passagem: "Este resíduo é dissolvido em água e o catalisador é retirado por filtração" O enunciado está nos dizendo que o resíduo a que ele se refere é o sal que se dissolveu e o catalisador que chegou ao final sem ser consumido.
E na passagem: "Este resíduo é dissolvido em água e o catalisador é retirado por filtração" O enunciado está nos dizendo que o resíduo a que ele se refere é o sal que se dissolveu e o catalisador que chegou ao final sem ser consumido.
____________________________________________
Thálisson.

Thálisson C- Monitor

- Mensagens : 3020
Data de inscrição : 19/02/2014
Idade : 27
Localização : Gurupi -TO
 Re: Estequiometria VI
Re: Estequiometria VI
Você está certo, desculpe a falta de atenção... química parece que não é pra mim :lThálisson C escreveu:Não Ashitaka, o catalisador não reagiu, ele apenas participou como acelerador da reação, tanto que eu nem coloquei MnO2 nas reações que apresentei.
E na passagem: "Este resíduo é dissolvido em água e o catalisador é retirado por filtração" O enunciado está nos dizendo que o resíduo a que ele se refere é o sal que se dissolveu e o catalisador que chegou ao final sem ser consumido.
Eu achei complicado entender qual é o tal resíduo. Pra mim poderia ser impureza + catalisador + sal ou qualquer combinação duas a duas desses 3. Isso da impureza deixou meio obscuro. Só dá pra ter certeza que fica o KCl, já que reage depois. Parece que o jeito é "adivinhar" e ver o que dá.

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 11/03/2013
Localização : São Paulo
 Re: Estequiometria VI
Re: Estequiometria VI
A química é pra vc sim cara! Você está muito melhor que eu quando comecei, eu não passava nem perto de fazer um exercício desse, kk 
E foi muito lógico seu questionamento da impureza.
E foi muito lógico seu questionamento da impureza.
____________________________________________
Thálisson.

Thálisson C- Monitor

- Mensagens : 3020
Data de inscrição : 19/02/2014
Idade : 27
Localização : Gurupi -TO
 Re: Estequiometria VI
Re: Estequiometria VI
Obrigado pela autoestima, parceiro!

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 11/03/2013
Localização : São Paulo
 Re: Estequiometria VI
Re: Estequiometria VI
Thálisson, esse exercício é antigo do IME e são conhecidos por não serem perfeitos. Hoje foi comentado sobre esse exercício e o enunciado está equivocado. 1,52 deveria ser a massa de 1,49 (KCl) + m(MnO2) + 0,55 (impureza). Resultaria numa massa negativa de catalisador. Subentende-se que ao aquecer, apenas o O2 do KClO3 é liberado. Mas para chegar ao resultado o jeito é fazer como você fez mesmo, só vim te avisar!

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 11/03/2013
Localização : São Paulo
Página 1 de 2 • 1, 2 
Página 1 de 2
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













