Estequiometria II
2 participantes
Página 1 de 1
 Estequiometria II
Estequiometria II
1 kg de uma mistura contendo somente NaCl, nitrato de potássio e sulfato de magnésio foi dissolvida em água e tratada com nitrato de prata. O precipitado de cloreto de prata pesou 1,435 g. O filtrado da precipitação do cloreto é tratado com nitrato de bário, dando um precipitado de sulfato de bário pesando 0,233 g. Qual a composição centesimal da mistura?
Não tenho muita vivência em química e o real problema acredito que seja não conhecer as reações. Agradeço se as apresentarem!
Não tenho muita vivência em química e o real problema acredito que seja não conhecer as reações. Agradeço se as apresentarem!

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 12/03/2013
Localização : São Paulo
 Re: Estequiometria II
Re: Estequiometria II
E aí Ashitaka. Questão difícil hein? Vamos lá.
Essa é a mistura inicial:
Sabemos, pelo enunciado, que o precipitado de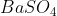 tem massa de 0,233g. Como cada 120g de
tem massa de 0,233g. Como cada 120g de 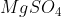 formam 233,5g de
formam 233,5g de 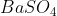 , basta uma regra de três para descobrir que 0,120g de
, basta uma regra de três para descobrir que 0,120g de 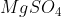 existiam na mistura inicial.
existiam na mistura inicial.
Sabemos, portanto, que existiam, na mistura inicial:
Por fim, calculando a composição centesimal da mistura:
is this it?
Essa é a mistura inicial:
Temos, pelo enunciado da questão, que o precipitado de 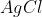 possui massa de 1,435g. A única reação que pode formar
possui massa de 1,435g. A única reação que pode formar 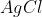 , com os componentes da mistura, é a seguinte, já balanceada:
, com os componentes da mistura, é a seguinte, já balanceada:
Como cada 58,5g de NaCl forma 143,5g de 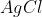 , basta uma regra de três para descobrir que 1,435g de
, basta uma regra de três para descobrir que 1,435g de 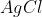 são formadas por uma reação com 0,585g de
são formadas por uma reação com 0,585g de 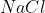 . Sabemos, portanto, que a quantia de
. Sabemos, portanto, que a quantia de 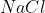 na mistura inicial é de 0,585g.
na mistura inicial é de 0,585g.
Vamos, agora, para a segunda parte da questão. Temos que alguma substância das que não reagiram com o 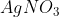 reage com
reage com _{2}) , formando 0,233g de
, formando 0,233g de 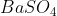 . A única substância que pode formar
. A única substância que pode formar 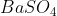 , em reação com
, em reação com _{2}) , das presentes na mistura, é o
, das presentes na mistura, é o 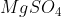 , reagindo seguindo a seguinte reação, já balanceada:
, reagindo seguindo a seguinte reação, já balanceada:
Sabemos, pelo enunciado, que o precipitado de
Sabemos, portanto, que existiam, na mistura inicial:
Por fim, calculando a composição centesimal da mistura:
is this it?
 Re: Estequiometria II
Re: Estequiometria II
Obrigado; analisando assim separadamente ficou mais fácil. Eu não sabia as reações que aconteciam, daí ficou uma bagunça saber o que acontecia.
Obrigado!!
Obrigado!!

Ashitaka- Monitor

- Mensagens : 4365
Data de inscrição : 12/03/2013
Localização : São Paulo
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














