Equação de Nernst
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Equação de Nernst
Equação de Nernst
Quando dois metais distintos (eletrodos) são imersos em uma solução condutora (eletrólito), produz-se uma célula ou uma pillha galvânica. A diferença de potencial fornecida pela célula pode ser calculada pela equação de Nernst
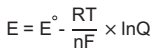
em que E é a diferença de potencial fornecida pela pilha; E" é o potencial padrão da pilha; R é a constante universal dos gases; n é o número de elétrons envolvidos na semirreação de oxidação ou redução; F é a constante de Faraday, e Q é quociente reacional, o qual fornece a razão entre as atividades dos produtos e dos reagentes envolvidos na reação global da pilha.
Com base no exposto acima, informe se é verdadeiro (V) ou falso (F) o que se afirma a seguir.
( ) Quanto maior for o tamanho da célula, maior será o potencial fornecido.
( ) Os materiais que compõem os eletrodos afetam o potencial gerado pela pilha.
( ) A concentração dos íons em solução não influencia o potencial fornecido pela pilha.
( ) A diferença de potencial gerada pela pilha varia com a temperatura da célula e com a composição do eletrólito.
De acordo com as afirmações, a sequência correta é
Alternativas
A)(V); (V); (F); (V).
B)(F); (F); (V); (F).
C)(F); (V); (F); (V).
D)(V); (F); (V); (F).
Resposta: C
Poderiam explicar cada assertiva?
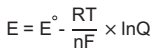
em que E é a diferença de potencial fornecida pela pilha; E" é o potencial padrão da pilha; R é a constante universal dos gases; n é o número de elétrons envolvidos na semirreação de oxidação ou redução; F é a constante de Faraday, e Q é quociente reacional, o qual fornece a razão entre as atividades dos produtos e dos reagentes envolvidos na reação global da pilha.
Com base no exposto acima, informe se é verdadeiro (V) ou falso (F) o que se afirma a seguir.
( ) Quanto maior for o tamanho da célula, maior será o potencial fornecido.
( ) Os materiais que compõem os eletrodos afetam o potencial gerado pela pilha.
( ) A concentração dos íons em solução não influencia o potencial fornecido pela pilha.
( ) A diferença de potencial gerada pela pilha varia com a temperatura da célula e com a composição do eletrólito.
De acordo com as afirmações, a sequência correta é
Alternativas
A)(V); (V); (F); (V).
B)(F); (F); (V); (F).
C)(F); (V); (F); (V).
D)(V); (F); (V); (F).
Resposta: C
Poderiam explicar cada assertiva?
Última edição por samuelbelembr@gmail.com em 7/1/2022, 3:13 pm, editado 1 vez(es)
samuelbelembr@gmail.com- Jedi

- Mensagens : 205
Data de inscrição : 04/10/2021
 Re: Equação de Nernst
Re: Equação de Nernst
I) Falsa. Em uma célula galvânica o que pode alterar o potencial é o eletrodo em si(o material da barra/solução + a concentração da solução), a temperatura e em que ponto do equilíbrio a reação está(que é a parte do ln Q na equação de Nernst), se você tiver uma célula gigante e uma pequena que tenham esses mesmos aspectos citados anteriormente, o potencial será o mesmo.
II) Verdadeira. Materiais diferentes terão potenciais de redução diferentes, afetando diretamente o potencial da pilha.
III) Falsa. Como é mostrado na equação de Nernst, o termo ln Q é influenciado diretamente pelas concentrações dos íons, alterando o potencial.
IV) Verdadeira. Novamente olhando para a equação de Nernst, o potencial varia com a temperatura e materiais diferentes tem potenciais de redução diferentes, o que altera o potencial.
Apenas para complementar, se uma pilha tivesse a equação abaixo, a equação de Nernst ficaria assim:
[latex] A^+ + B\rightleftharpoons A + B^+ [/latex]
[latex] E=E_0-\frac{RT}{F}ln(\frac{[A].[B^+]}{[A^+].[B]}) [/latex]
II) Verdadeira. Materiais diferentes terão potenciais de redução diferentes, afetando diretamente o potencial da pilha.
III) Falsa. Como é mostrado na equação de Nernst, o termo ln Q é influenciado diretamente pelas concentrações dos íons, alterando o potencial.
IV) Verdadeira. Novamente olhando para a equação de Nernst, o potencial varia com a temperatura e materiais diferentes tem potenciais de redução diferentes, o que altera o potencial.
Apenas para complementar, se uma pilha tivesse a equação abaixo, a equação de Nernst ficaria assim:
[latex] A^+ + B\rightleftharpoons A + B^+ [/latex]
[latex] E=E_0-\frac{RT}{F}ln(\frac{[A].[B^+]}{[A^+].[B]}) [/latex]

Leonardo Mariano- Monitor

- Mensagens : 506
Data de inscrição : 11/11/2018
Idade : 22
Localização : Criciúma/SC
 Tópicos semelhantes
Tópicos semelhantes» Equação de Nernst
» CIAAR - Equação de nernst
» ITA 2014 - Equação de Nernst
» Eletroquímica - Equação de Nernst
» Verifique se a equação dada é exata (Equação Diferencial)
» CIAAR - Equação de nernst
» ITA 2014 - Equação de Nernst
» Eletroquímica - Equação de Nernst
» Verifique se a equação dada é exata (Equação Diferencial)
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













