(Cespe 2015) Química
2 participantes
Página 1 de 1
 (Cespe 2015) Química
(Cespe 2015) Química
Uma amostra de 50 mL de chuva ácida, composta apenas de água e H2SO4, foi titulada com uma solução padrão de NaOH com concentração 2,00 × 10^3 mol/L. Quando atingido o ponto de equivalência da titulação, haviam sido gastos 12,0 mL da solução de NaOH. Considerando essa situação e, ainda, que as soluções apresentem comportamento ideal, que a constante de autoionização da água seja igual a 1,0 × 10^14 e que log 5 = 0,70.
Calcule a concentração de H2SO4 na amostra de chuva ácida. Multiplique o resultado obtido por 10^5. (Gabarito: 24)
Como proceder essa resolução amigos
Calcule a concentração de H2SO4 na amostra de chuva ácida. Multiplique o resultado obtido por 10^5. (Gabarito: 24)
Como proceder essa resolução amigos

VctMR- Jedi

- Mensagens : 255
Data de inscrição : 11/05/2018
Idade : 24
Localização : Brasíla
 Re: (Cespe 2015) Química
Re: (Cespe 2015) Química
Olá,
a reação é a seguinte:
Balanceando, temos:
A reação acontece até não haver 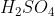 remanescente. Encontrando quantos mols de
remanescente. Encontrando quantos mols de 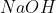 reagiram:
reagiram:
Encontrando a quantidade de mols de 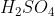 que reagiram:
que reagiram:
da reação,
Ou seja, 12 mols de 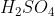 em 50 mL de chuva:
em 50 mL de chuva:
Como o enunciado pede pra multiplicar por 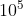 , então:
, então:
Confira, por favor, o gabarito e o enunciado.

Tess- Matador

- Mensagens : 124
Data de inscrição : 04/05/2018
Idade : 25
Localização : Brasil
 Tópicos semelhantes
Tópicos semelhantes» (Cespe 2015) Física - Óptica
» (Cespe 2014) Química
» (Cespe 2015) Análise Combinatória
» (Cespe 2015) Física Ondulatória
» (Cespe 2015) Geometria Espacial
» (Cespe 2014) Química
» (Cespe 2015) Análise Combinatória
» (Cespe 2015) Física Ondulatória
» (Cespe 2015) Geometria Espacial
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












