ESTEQUIOMETRIA
2 participantes
Página 1 de 1
 ESTEQUIOMETRIA
ESTEQUIOMETRIA
(PUC-MG) Dada a reação: ferro + ácido clorídrico à cloreto férrico + hidrogênio o número de moléculas de gás hidrogênio, produzidas pela reação de 112 g de ferro, é igual a: a) 1,5 b) 3,0 c) 9,0 . 1023 d) 1,8' 1024 e) 3,0 . 1024
resposta: letra d 1,8 . 1024
NÃO CONSIGO FAZER O BALANCEAMENTO, O FERRO É DA FAMILIA 8B COM DOIS ELETRONS NA ULTIMA CAMADA ISSO SIGINIFICA QUE ELE PODE DOAR ATÉ 2 ELETRONS, CERTO?
resposta: letra d 1,8 . 1024
NÃO CONSIGO FAZER O BALANCEAMENTO, O FERRO É DA FAMILIA 8B COM DOIS ELETRONS NA ULTIMA CAMADA ISSO SIGINIFICA QUE ELE PODE DOAR ATÉ 2 ELETRONS, CERTO?
joão.tr- Iniciante
- Mensagens : 8
Data de inscrição : 17/06/2014
Idade : 25
Localização : mucuge, bahia, brasil
 Re: ESTEQUIOMETRIA
Re: ESTEQUIOMETRIA
Olá novamente kkkkk A equação balanceada fica dessa maneira:
Fe + 3HCl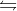 FeCl₃ +
FeCl₃ +  H₂
H₂
Temos FeCl₃ porque se trata de Cloreto Férrico, ou Cloreto de Ferro III em que o Fe se configura no cátion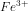 doando, portanto, 3 elétrons e não 2.
doando, portanto, 3 elétrons e não 2.
Fazendo a estequiometria:
Fe + 3HCl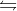 FeCl₃ +
FeCl₃ +  H₂
H₂
56g------------------3g
112g-----------------6g
Em 112g de Fe, temos, então, 2 mols de Fe; se temos 2 mols de Fe, temos 3 mols de H₂ ( x 2).
x 2).
Para calcular a quantidade de moléculas, multiplico a quantidade de mols pela constante de avogrado 6x10²³:
3 mols x 6x10²³= 1,8x10²⁴ moléculas.
Fe + 3HCl
Temos FeCl₃ porque se trata de Cloreto Férrico, ou Cloreto de Ferro III em que o Fe se configura no cátion
Fazendo a estequiometria:
Fe + 3HCl
56g------------------3g
112g-----------------6g
Em 112g de Fe, temos, então, 2 mols de Fe; se temos 2 mols de Fe, temos 3 mols de H₂ (
Para calcular a quantidade de moléculas, multiplico a quantidade de mols pela constante de avogrado 6x10²³:
3 mols x 6x10²³= 1,8x10²⁴ moléculas.

Emily Stephanny- Iniciante
- Mensagens : 35
Data de inscrição : 12/09/2014
Idade : 26
Localização : Cuiabá, MT, Brasil
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













