fórmula de sais
2 participantes
Página 1 de 1
 fórmula de sais
fórmula de sais
sulfito de cálcio = sulfito 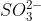 e cálcio
e cálcio 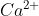 = CaSO3.
= CaSO3.
Alguém pode me explicar de onde saiu aquele 3 debaixo do O do sulfito.
Alguém pode me explicar de onde saiu aquele 3 debaixo do O do sulfito.

puiff- Mestre Jedi

- Mensagens : 547
Data de inscrição : 17/02/2012
Idade : 29
Localização : Jacareí - SP
 Re: fórmula de sais
Re: fórmula de sais
O enxofre é o átomo central, pois é o que está em menor quantidade (1 átomo por ânion) e é aquele que possui a maior capacidade de ligações químicas (6 ligações). Logo, tem-se que:

O oxigênio da dativa não ganha elétron e os outros dois oxigênios, por serem muito eletronegativos, ficam com 2 elétrons, formando o ânion sulfito.
OBS: perceba que ainda sobram 2 elétrons "soltos" na camada de valência do enxofre, ou seja, justamente os elétrons que irão se juntar a outro oxigênio para formar o sulfato (SO4-2).


O oxigênio da dativa não ganha elétron e os outros dois oxigênios, por serem muito eletronegativos, ficam com 2 elétrons, formando o ânion sulfito.
OBS: perceba que ainda sobram 2 elétrons "soltos" na camada de valência do enxofre, ou seja, justamente os elétrons que irão se juntar a outro oxigênio para formar o sulfato (SO4-2).
![[Planck]³](https://2img.net/u/2713/85/25/58/avatars/19563-97.jpg)
[Planck]³- Fera

- Mensagens : 673
Data de inscrição : 11/02/2012
Idade : 31
Localização : Mossoró-RN
 Re: fórmula de sais
Re: fórmula de sais
Eu ainda não entendi muito bem :[
não entendi porque vc falou de sulfato ali.
não entendi porque vc falou de sulfato ali.

puiff- Mestre Jedi

- Mensagens : 547
Data de inscrição : 17/02/2012
Idade : 29
Localização : Jacareí - SP
 Re: fórmula de sais
Re: fórmula de sais
Muita calma nessa hora, puiff !!! Vamos lá:
Percebe os dois ''xizinhos'' no enxofre ? Pois é, são as representações de elétrons que sobraram. Se por acaso o ambiente estiver abundante em oxigênio ainda dá para fazer mais uma ligação dativa com o oxigênio formando o sulfato (SO4-2).
Ou seja, o enxofre pode ganhar 2 elétrons, tornando-se o sulfeto S-2 (lembre-se que ele é da família 6A e ganha 2 elétrons), pode ganhar 2 elétrons e formar o SO3-2 e ,enfim, pode ganhar 2 elétrons e formar o SO4-2.
Qualquer dúvida que tenha ficado pode perguntar viu, não se acanhe.
Abraços.
Percebe os dois ''xizinhos'' no enxofre ? Pois é, são as representações de elétrons que sobraram. Se por acaso o ambiente estiver abundante em oxigênio ainda dá para fazer mais uma ligação dativa com o oxigênio formando o sulfato (SO4-2).
Ou seja, o enxofre pode ganhar 2 elétrons, tornando-se o sulfeto S-2 (lembre-se que ele é da família 6A e ganha 2 elétrons), pode ganhar 2 elétrons e formar o SO3-2 e ,enfim, pode ganhar 2 elétrons e formar o SO4-2.
Qualquer dúvida que tenha ficado pode perguntar viu, não se acanhe.
Abraços.
![[Planck]³](https://2img.net/u/2713/85/25/58/avatars/19563-97.jpg)
[Planck]³- Fera

- Mensagens : 673
Data de inscrição : 11/02/2012
Idade : 31
Localização : Mossoró-RN
 Tópicos semelhantes
Tópicos semelhantes» sais formula
» Formula Sais
» Explicação fórmula dos sais
» Sais e fórmula química
» Fórmula mínima e nome dos sais
» Formula Sais
» Explicação fórmula dos sais
» Sais e fórmula química
» Fórmula mínima e nome dos sais
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













