Estequiometria
2 participantes
Página 1 de 1
 Estequiometria
Estequiometria
A amostra de calcário apresenta 75% de pureza em carbonato de cálcio (CaCO3). Fazendo-se reagir 20,0g dessa amostra com ácido clorídrico em excesso, o volume (em litros) de gás liberado a 127oC e 1 atm é:
a) 4,92L
b) 9,84L
c) 15,00L
d) 22,4L
e) 49,20L
Gab: letra "A"
Dúvida: Não consegui chegar nesse resultado.
a) 4,92L
b) 9,84L
c) 15,00L
d) 22,4L
e) 49,20L
Gab: letra "A"
Dúvida: Não consegui chegar nesse resultado.
Edirlei Elder- Padawan

- Mensagens : 55
Data de inscrição : 05/03/2022
Idade : 20
Localização : Angra, RJ
 Re: Estequiometria
Re: Estequiometria
Olá Edirlei;
Montando a equação química, temos:

Assim, fazendo a proporção estequiométrica:
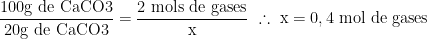
Para o cálculo de volume iremos recorrer a Equação de Clapeyron, dessa forma, nas respectivas condições, temos:
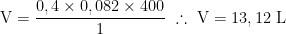
Mas esse volume acontece na situação ideal com rendimento de 100%, em 75%, temos:
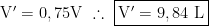
Também estou chegando em outro valor, creio que o gabarito esteja errado, o correto é letra b).
Montando a equação química, temos:
Assim, fazendo a proporção estequiométrica:
Para o cálculo de volume iremos recorrer a Equação de Clapeyron, dessa forma, nas respectivas condições, temos:
Mas esse volume acontece na situação ideal com rendimento de 100%, em 75%, temos:
Também estou chegando em outro valor, creio que o gabarito esteja errado, o correto é letra b).

qedpetrich- Monitor

- Mensagens : 2496
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
 Re: Estequiometria
Re: Estequiometria
Desculpe, mas ainda fiquei com uma dúvida!qedpetrich escreveu:Olá Edirlei;
Montando a equação química, temos:
Assim, fazendo a proporção estequiométrica:
Para o cálculo de volume iremos recorrer a Equação de Clapeyron, dessa forma, nas respectivas condições, temos:
Mas esse volume acontece na situação ideal com rendimento de 100%, em 75%, temos:
Também estou chegando em outro valor, creio que o gabarito esteja errado, o correto é letra b).
De onde veio esses 2 mols de gases?
Edirlei Elder- Padawan

- Mensagens : 55
Data de inscrição : 05/03/2022
Idade : 20
Localização : Angra, RJ
 Re: Estequiometria
Re: Estequiometria
Da proporção estequiométrica, quando reagimos 1 mol de carbonato de cálcio (CaCO3) com 2 mols de ácido clorídrico (HCl), temos a produção de 1 mol de cloreto de cálcio (CaCl2) com 1 mol de água (H2O) e 1 mol de dióxido de carbono (CO2). Tanto a água como o dióxido de carbono se encontram na forma gasosa, por isso considerei 2 mols de gases (Somente o dióxido de carbono se encontra na forma de gás). Conseguiu entender? Qualquer dúvida mande mensagem. 
Última edição por qedpetrich em Sex 18 Mar 2022, 16:24, editado 1 vez(es)

qedpetrich- Monitor

- Mensagens : 2496
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
 Re: Estequiometria
Re: Estequiometria
Pensando bem aqui a água na verdade está na forma de vapor não na forma de gás, então da minha conclusão somente 1 mol está em estado gasoso, aí sim fecha com o gabarito. Desculpe pela confusão, já editei.
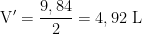

qedpetrich- Monitor

- Mensagens : 2496
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













