Teoria cinética dos gases
2 participantes
PiR2 :: Física :: Mecânica dos Fluidos
Página 1 de 1
 Teoria cinética dos gases
Teoria cinética dos gases
A que temperatura a energia cinética média de uma molécula de um gás ideal é igual a 0,01 eV?
Última edição por nessinhanl em Dom 29 Ago 2021, 00:26, editado 1 vez(es)
nessinhanl- Iniciante
- Mensagens : 35
Data de inscrição : 15/08/2021
Localização : Rio de Janeiro, RJ - Brasil
 Re: Teoria cinética dos gases
Re: Teoria cinética dos gases
Bom dia nesssinhanl.
Aplicando a energia cinética de um gás ideal, temos:
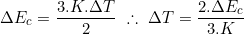
Se 1 eV = 1,6 x 10⁻¹⁹ J. Então 0,01 eV = 1,6 x 10⁻²¹ J. Sendo K a constante de boltzmann; K = 1,38 x 10⁻²³ J.K⁻¹. Mera substituição:
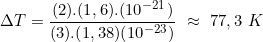
Perceba que essa equação possui diversas equivalências, eu poderia ter calculado à partir da informação do número de mols, veja:

Onde n é o número de mols e R é a constante universal dos gases; R = 8,31 J.K⁻¹.mol⁻¹. Extraindo as informações do enunciado, podemos chegar a conclusão que se em 1 mol temos 6 x 10 ²³ moléculas, em uma molécula temos apenas um valor unitário, ou seja, n = 1/(6,02 x 10²³) mol.
Substituindo na equação proposta:
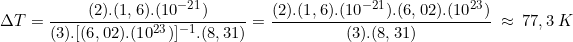
Essa equação, ainda poderia ser estendida à casos de pressão e volume, é fácil perceber que pela equação de Clapeyron; nR∆T = PV, ficando com:
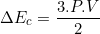
Você possui conhecimento sobre o gabarito? Se sim, poste, por favor! Espero ter ajudado.
Aplicando a energia cinética de um gás ideal, temos:
Se 1 eV = 1,6 x 10⁻¹⁹ J. Então 0,01 eV = 1,6 x 10⁻²¹ J. Sendo K a constante de boltzmann; K = 1,38 x 10⁻²³ J.K⁻¹. Mera substituição:
Perceba que essa equação possui diversas equivalências, eu poderia ter calculado à partir da informação do número de mols, veja:
Onde n é o número de mols e R é a constante universal dos gases; R = 8,31 J.K⁻¹.mol⁻¹. Extraindo as informações do enunciado, podemos chegar a conclusão que se em 1 mol temos 6 x 10 ²³ moléculas, em uma molécula temos apenas um valor unitário, ou seja, n = 1/(6,02 x 10²³) mol.
Substituindo na equação proposta:
Essa equação, ainda poderia ser estendida à casos de pressão e volume, é fácil perceber que pela equação de Clapeyron; nR∆T = PV, ficando com:
Você possui conhecimento sobre o gabarito? Se sim, poste, por favor! Espero ter ajudado.

qedpetrich- Monitor

- Mensagens : 2495
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
nessinhanl gosta desta mensagem
 Re: Teoria cinética dos gases
Re: Teoria cinética dos gases
Muito obrigada! No gabarito era essa resposta mesmo (77,3 k).
nessinhanl- Iniciante
- Mensagens : 35
Data de inscrição : 15/08/2021
Localização : Rio de Janeiro, RJ - Brasil
qedpetrich gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» A TEORIA CINÉTICA DOS GASES
» Teoria cinética dos gases
» Teoria cinética dos gases
» Teoria cinética dos gases
» Teoria Cinética dos Gases
» Teoria cinética dos gases
» Teoria cinética dos gases
» Teoria cinética dos gases
» Teoria Cinética dos Gases
PiR2 :: Física :: Mecânica dos Fluidos
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













