Termoquímica: Gráficos Termocinéticos
3 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Termoquímica: Gráficos Termocinéticos
Termoquímica: Gráficos Termocinéticos
(UEM-PR) Considerando-se o gráfico a seguir, que representa uma reação genérica na qual podem ser obtidos, simultaneamente, dois produtos diferentes, assinale o que for CORRETO.
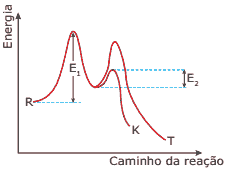
01. Os compostos K e T são obtidos através de uma reação exotérmica.
02. A velocidade de formação do produto T é menor que a do produto K.
04. O produto T é mais estável que o produto K.
08. A energia representada pela letra E1 corresponde à energia de ativação para a formação de um composto intermediário, e a energia representada pela letra E2 corresponde à energia de ativação para a formação do produto K.
16. Se a reação tiver início a partir do mesmo reagente R, é possível supor que o produto K se formará primeiro, mas que o mesmo se converterá, espontaneamente, no produto T.
32. O gráfico evidencia a formação de um intermediário comum.
64. A reação apresentada pela curva do produto T pode ser dita catalisada, enquanto a do produto K é não catalisada.
Minha dúvida ocorre em relação ao item 04. Como saber qual dos produtos é mais estável?

01. Os compostos K e T são obtidos através de uma reação exotérmica.
02. A velocidade de formação do produto T é menor que a do produto K.
04. O produto T é mais estável que o produto K.
08. A energia representada pela letra E1 corresponde à energia de ativação para a formação de um composto intermediário, e a energia representada pela letra E2 corresponde à energia de ativação para a formação do produto K.
16. Se a reação tiver início a partir do mesmo reagente R, é possível supor que o produto K se formará primeiro, mas que o mesmo se converterá, espontaneamente, no produto T.
32. O gráfico evidencia a formação de um intermediário comum.
64. A reação apresentada pela curva do produto T pode ser dita catalisada, enquanto a do produto K é não catalisada.
Minha dúvida ocorre em relação ao item 04. Como saber qual dos produtos é mais estável?
Última edição por eivitordias em Qua 8 Abr - 12:35, editado 4 vez(es)

eivitordias- Jedi

- Mensagens : 302
Data de inscrição : 07/04/2020
Localização : Santa Catarina, Brasil
 Re: Termoquímica: Gráficos Termocinéticos
Re: Termoquímica: Gráficos Termocinéticos
Fica mais difícil sem o gráfico, mas o produto mais estável, geralmente, é aquele que possui menor nível energético.
André Meneses- Recebeu o sabre de luz

- Mensagens : 173
Data de inscrição : 12/07/2016
Idade : 22
Localização : Natal - RN
 Re: Termoquímica: Gráficos Termocinéticos
Re: Termoquímica: Gráficos Termocinéticos
André Meneses escreveu:Fica mais difícil sem o gráfico, mas o produto mais estável, geralmente, é aquele que possui menor nível energético.
Perdão, já coloquei a imagem novamente. Acredito que o motivo seja esse mesmo, pelo fato do produto T apresentar menor entalpia, consequentemente será mais estável. Menor energia implica em maior estabilidade

eivitordias- Jedi

- Mensagens : 302
Data de inscrição : 07/04/2020
Localização : Santa Catarina, Brasil
 Re: Termoquímica: Gráficos Termocinéticos
Re: Termoquímica: Gráficos Termocinéticos
poderiam explicar os itens,08,32,16 e 64?

GuilhermeSS- Jedi

- Mensagens : 226
Data de inscrição : 18/04/2020
Idade : 23
Localização : Teresina, Piauí
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














