Titulação
4 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Titulação
Titulação
Em um experimento, uma amostra de 10 mL de um produto químico comercial que contém hidróxido de cálcio foi completamente neutralizada por 5 mL de solução aquosa de ácido clorídrico com concentração igual a 0,01 mol.L-1 . Escreva a equação química completa e balanceada dessa reação de neutralização. Em seguida, calcule a concentração, em g.L-1 , de hidróxido de cálcio presente na amostra do produto comercial.
Gabarito: C = 0,185 g/L
Como resolve essa questão através da formula de cálculo de titulação?
Gabarito: C = 0,185 g/L
Como resolve essa questão através da formula de cálculo de titulação?
Última edição por maiarads em Ter 24 Set 2019, 22:03, editado 1 vez(es)

maiarads- Padawan

- Mensagens : 72
Data de inscrição : 26/08/2019
Idade : 22
Localização : Uberlândia
 Re: Titulação
Re: Titulação
1) Anote os dados de cada reagente
2) Escreva a reação balanceada
3) Descubra a proporção esteq. em mols ácido e base
4) Relacione o n de mols da base titulada com o volume titulado para achar essa informação em 1L
Ca(OH)2 -> Vb=10ml foi titulado
HCl -> Va=5.10^-3L foi titulante e Ma=10^-2mol.L-1
Ca(OH)2 + 2HCl ---> CaCl2 + 2H2O
1mols ----- 2mols
n -------- Ma.Va (5.10^-5)
n base = 2,5.10^-5
Isso é o que se tem de base em mols, em 10ml de solução básica que foi titulada.
Descubra o que tem em 1L, pois o resultado da estequiometria vale para o volume usado para a base titulada, no caso 10ml:
10ml -- 2,5.10^-5
1L ----- M
Mb=2,5.10^-3 mol/L
Temos a molaridade, agora em 1L. Achando a concentração
2,5.10^-3 mol --- xg
1 mol ---------- 74g
x=0,185g
C= 0,185g/L
2) Escreva a reação balanceada
3) Descubra a proporção esteq. em mols ácido e base
4) Relacione o n de mols da base titulada com o volume titulado para achar essa informação em 1L
Ca(OH)2 -> Vb=10ml foi titulado
HCl -> Va=5.10^-3L foi titulante e Ma=10^-2mol.L-1
Ca(OH)2 + 2HCl ---> CaCl2 + 2H2O
1mols ----- 2mols
n -------- Ma.Va (5.10^-5)
n base = 2,5.10^-5
Isso é o que se tem de base em mols, em 10ml de solução básica que foi titulada.
Descubra o que tem em 1L, pois o resultado da estequiometria vale para o volume usado para a base titulada, no caso 10ml:
10ml -- 2,5.10^-5
1L ----- M
Mb=2,5.10^-3 mol/L
Temos a molaridade, agora em 1L. Achando a concentração
2,5.10^-3 mol --- xg
1 mol ---------- 74g
x=0,185g
C= 0,185g/L

Raquel Valadão- Mestre Jedi

- Mensagens : 523
Data de inscrição : 04/04/2017
Localização : Bahia
 Re: Titulação
Re: Titulação
Um jeito diferente(com fórmula):
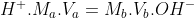
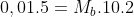
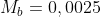 mol/L
mol/L
1 mol Na(OH)2 ----- 74 gramas
0,0025 ----- x gramas
x = 0,185g = 0,0025 mol Na(OH)2
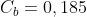 g/L
g/L
1 mol Na(OH)2 ----- 74 gramas
0,0025 ----- x gramas
x = 0,185g = 0,0025 mol Na(OH)2

Dr.Astro- Mestre Jedi

- Mensagens : 516
Data de inscrição : 12/06/2019
Localização : Brasil
 Re: Titulação
Re: Titulação
Ca(OH)2 * Era o método mais rápido de se resolver a questãoDr.Astro escreveu:Um jeito diferente(com fórmula):mol/L
1 mol Na(OH)2 ----- 74 gramas
0,0025 ----- x gramas
x = 0,185g = 0,0025 mol Na(OH)2g/L

folettinhomed- Mestre Jedi

- Mensagens : 988
Data de inscrição : 23/02/2019
Idade : 23
Localização : Santa Cruz do Sul, RS, Brasil
 Re: Titulação
Re: Titulação
@Dr.astro na equação balanceada são 2HCl, logo não seria 2 H+ ?
e posso usar essa formula em toda titulação ou apenas se o reagentes forem uma base e um ácido?
e posso usar essa formula em toda titulação ou apenas se o reagentes forem uma base e um ácido?

maiarads- Padawan

- Mensagens : 72
Data de inscrição : 26/08/2019
Idade : 22
Localização : Uberlândia
 Re: Titulação
Re: Titulação
Não. O "2" são os H+/OH- ionizáveis.
Como é Na(OH)2 então há 2OH ionizáveis para cada H. Por isso o 2 no lado da base. OH-=2
Essa fórmula só funciona com titulação ácido-base.
Como é Na(OH)2 então há 2OH ionizáveis para cada H. Por isso o 2 no lado da base. OH-=2
Essa fórmula só funciona com titulação ácido-base.

Dr.Astro- Mestre Jedi

- Mensagens : 516
Data de inscrição : 12/06/2019
Localização : Brasil
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














