Cinética Química I
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Cinética Química I
Cinética Química I
(UFPE) O gráfico ilustra a variação da energia livre ao longo de uma reação química, que ocorre em duas etapas:
Etapa I: A --> B
Etapa II: B --> C
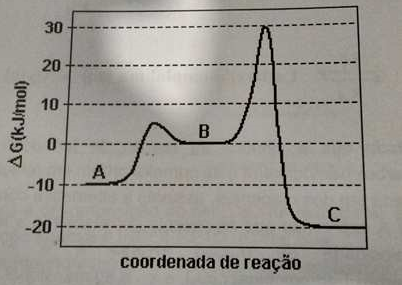
A partir da análise do gráfico julgue as alternativas a seguir:
() a etapa I é espontânea.
() a etapa II é a etapa determinante da velocidade da reação global.
() a substância B é um intermediário da reação.
() a reação global A --> C é espontânea
() a reação inversa C --> B apresenta energia livre de Gibbs de ativação igual a 20 kj/mol
Gabarito: F V V V F
Minhas dúvidas são em relação aos itens em negrito. Alguém poderia me explicar detalhadamente?
Obrigado.
Etapa I: A --> B
Etapa II: B --> C

A partir da análise do gráfico julgue as alternativas a seguir:
() a etapa I é espontânea.
() a etapa II é a etapa determinante da velocidade da reação global.
() a substância B é um intermediário da reação.
() a reação global A --> C é espontânea
() a reação inversa C --> B apresenta energia livre de Gibbs de ativação igual a 20 kj/mol
Gabarito: F V V V F
Minhas dúvidas são em relação aos itens em negrito. Alguém poderia me explicar detalhadamente?
Obrigado.

Orihara- Mestre Jedi

- Mensagens : 699
Data de inscrição : 18/09/2014
Idade : 28
Localização : Santa Catarina
 Re: Cinética Química I
Re: Cinética Química I
Na ordem das que você possui dúvidas ,
1 - Falsa , reação espontâneas tem energia livre de Gibbs negativa e como está é uma função de estado, ou seja, depende do estado inicial e final e como a etapa 1 é de A----> B deu positivo , não , não é espontâneo.
2- verdadeira ,
Etapa 1 - A---->B
Etapa 2 - B---->C
A reação global é a "soma" das duas , portanto :
A----->C
3-Falsa , a energia de ativação é tamanho do monte que você terá que percorrer na etapa dada , vulgarmente falando
Na etapa : C---->B , por exemplo , a energia interna é 50kj/mol.
1 - Falsa , reação espontâneas tem energia livre de Gibbs negativa e como está é uma função de estado, ou seja, depende do estado inicial e final e como a etapa 1 é de A----> B deu positivo , não , não é espontâneo.
2- verdadeira ,
Etapa 1 - A---->B
Etapa 2 - B---->C
A reação global é a "soma" das duas , portanto :
A----->C
3-Falsa , a energia de ativação é tamanho do monte que você terá que percorrer na etapa dada , vulgarmente falando
Na etapa : C---->B , por exemplo , a energia interna é 50kj/mol.

Matheus Tsilva- Fera

- Mensagens : 1167
Data de inscrição : 16/07/2015
Idade : 25
Localização : Uberaba, MG
 Re: Cinética Química I
Re: Cinética Química I
Obrigado pelas explicações, Matheus.

Orihara- Mestre Jedi

- Mensagens : 699
Data de inscrição : 18/09/2014
Idade : 28
Localização : Santa Catarina
 Tópicos semelhantes
Tópicos semelhantes» Cinética Química - Leis integrais da Cinética
» Cinética Química II
» Cinética Química
» Cinética química
» cinetica quimica
» Cinética Química II
» Cinética Química
» Cinética química
» cinetica quimica
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













