dúvida- termoquímica.
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 dúvida- termoquímica.
dúvida- termoquímica.
Coloque a s reações mencionadas abaixo em ordem crescente de liberação de calor, indicando esse fato em um gráfico de entalpia.
S (s) + O2 (g) -> SO2 (g) ∆H1
S (l) + O2 (g) -> SO2 (g) ∆H2
S (g) + O2 (g) -> SO2 (g) ∆H3
resolução:
|∆H1| < |∆H2| < |∆H3|

minha dúvida: Sei que o ∆H aumenta na seguinte relação sólido > líquido > gás, não entendi porque na resolução do livro do Feltre está o contrário... :scratch:
S (s) + O2 (g) -> SO2 (g) ∆H1
S (l) + O2 (g) -> SO2 (g) ∆H2
S (g) + O2 (g) -> SO2 (g) ∆H3
resolução:
|∆H1| < |∆H2| < |∆H3|

minha dúvida: Sei que o ∆H aumenta na seguinte relação sólido > líquido > gás, não entendi porque na resolução do livro do Feltre está o contrário... :scratch:
mari- Estrela Dourada

- Mensagens : 1134
Data de inscrição : 01/09/2015
Idade : 26
Localização : São Paulo
 Re: dúvida- termoquímica.
Re: dúvida- termoquímica.
Apenas analise o gráfico, observe que o ∆H do enxofre gasoso é maior que o do liquido que por sua vez é maior do que do sólido ...
Então de fato ocorre maior liberação no estado gasoso ....
Agora se analisarmos do modo o qual você afirmou, estaria incorreto.
O correto seria que o ∆H aumenta da seguinte maneira: solido < líquido < gás
Quando eu me confundo, eu costumo a fazer o seguinte gráfico, simplificadamente para relembrar-me.

Observe que quando eu "puxo" a seta lá no estádo gasoso, ela é bem maior do que no estado líquido, onde podemos concluir que o ∆H no estado gasoso é maior que no liquido .... Quando temos a seta para cima representa uma reação endotérmica, consequentemente para baixo uma exotérmica.
Espero que fique claro, um grande abraço!
Então de fato ocorre maior liberação no estado gasoso ....
Agora se analisarmos do modo o qual você afirmou, estaria incorreto.
O correto seria que o ∆H aumenta da seguinte maneira: solido < líquido < gás
Quando eu me confundo, eu costumo a fazer o seguinte gráfico, simplificadamente para relembrar-me.

Observe que quando eu "puxo" a seta lá no estádo gasoso, ela é bem maior do que no estado líquido, onde podemos concluir que o ∆H no estado gasoso é maior que no liquido .... Quando temos a seta para cima representa uma reação endotérmica, consequentemente para baixo uma exotérmica.
Espero que fique claro, um grande abraço!

Shino- Jedi

- Mensagens : 245
Data de inscrição : 18/04/2015
Idade : 26
Localização : Londrina, Paraná.
 Re: dúvida- termoquímica.
Re: dúvida- termoquímica.
Shino, olha oq tenho do livro
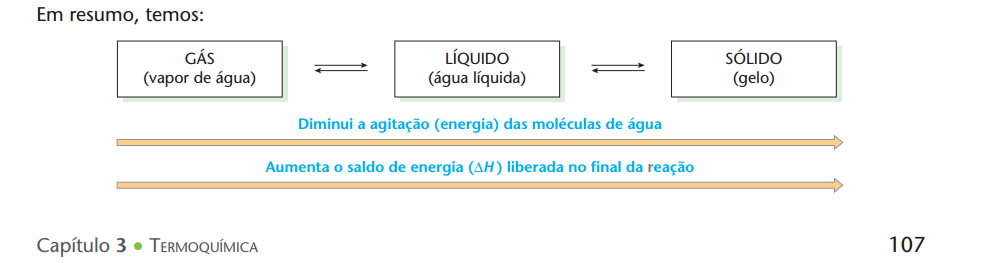
o ∆H não seria sólido > líquido > gás ?

o ∆H não seria sólido > líquido > gás ?
mari- Estrela Dourada

- Mensagens : 1134
Data de inscrição : 01/09/2015
Idade : 26
Localização : São Paulo
 Re: dúvida- termoquímica.
Re: dúvida- termoquímica.
Está fazendo uma interpretação errada mapll, observe que -----> "aumenta o saldo de energia (∆H) LIBERADA no final da reação" ou seja isso não significa que o ∆H do sólido > líquido > gás, e sim que o SALDO ∆H do sólido > líquido > gás, o que é claro de se notar no gráfico que eu proporcionei, pelo fato da LIBERAÇÃO de energia ser um processo exotérmico. Espero que fique claro. Abraço!

Shino- Jedi

- Mensagens : 245
Data de inscrição : 18/04/2015
Idade : 26
Localização : Londrina, Paraná.
 Re: dúvida- termoquímica.
Re: dúvida- termoquímica.
Entendi! Obrigada, Shino 
mari- Estrela Dourada

- Mensagens : 1134
Data de inscrição : 01/09/2015
Idade : 26
Localização : São Paulo
 Tópicos semelhantes
Tópicos semelhantes» TERMOQUÍMICA - dúvida
» dúvida termoquímica
» Dúvida de termoquímica
» duvida termoquimica
» Dúvida termoquimica.
» dúvida termoquímica
» Dúvida de termoquímica
» duvida termoquimica
» Dúvida termoquimica.
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













