(UNESP) Eletroquímica e Reação química
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 (UNESP) Eletroquímica e Reação química
(UNESP) Eletroquímica e Reação química
O peróxido de hidrogênio (H2O2) pode participar de reações de oxirredução como oxidante ou como redutor. Por exemplo, em meio ácido, íons dicromato  são reduzidos a íons crômico (Cr3+) pelo peróxido de hidrogênio, conforme a reação representada pela equação:
são reduzidos a íons crômico (Cr3+) pelo peróxido de hidrogênio, conforme a reação representada pela equação:

Escreva a equação química balanceada da semi-reação de redução do peróxido de hidrogênio à água em meio ácido.
Resposta:

Gostaria de saber se minha resolução está correta e se H+ e H3O+ são a mesma coisa.
Obrigada !
!
 são reduzidos a íons crômico (Cr3+) pelo peróxido de hidrogênio, conforme a reação representada pela equação:
são reduzidos a íons crômico (Cr3+) pelo peróxido de hidrogênio, conforme a reação representada pela equação:
Escreva a equação química balanceada da semi-reação de redução do peróxido de hidrogênio à água em meio ácido.
Resposta:

Gostaria de saber se minha resolução está correta e se H+ e H3O+ são a mesma coisa.
Obrigada

Giovana Martins- Grande Mestre

- Mensagens : 7601
Data de inscrição : 15/05/2015
Idade : 23
Localização : São Paulo
 Re: (UNESP) Eletroquímica e Reação química
Re: (UNESP) Eletroquímica e Reação química
Eu diria que a reação correta é:
H2O2 + 2H^+ + 2e^- ---> 2H2O
Pesquisei a questão na internet e achei respostas diferentes (H2O2 ---> H2O + 1/2O2), mas isso seria uma auto-oxirredução (desproporcionamento) e não uma redução. Então fui atrás de dados em inglês, e achei que a minha resposta está mais correta.
Contudo, não sou o dono da verdade. Posso estar errado, mas acho que é isso aí.
PS: sua resposta não está correta pois nela, o H2O2 não sofreu redução, mas sim desproporcionamento. Além disso, a reação tem de produzir ÁGUA e não hidrônio.
PS2: sim, H^+ e H3O^+ são a mesma coisa.
Espero ter lhe ajudado, Giovana. Qualquer dúvida é só perguntar!
H2O2 + 2H^+ + 2e^- ---> 2H2O
Pesquisei a questão na internet e achei respostas diferentes (H2O2 ---> H2O + 1/2O2), mas isso seria uma auto-oxirredução (desproporcionamento) e não uma redução. Então fui atrás de dados em inglês, e achei que a minha resposta está mais correta.
Contudo, não sou o dono da verdade. Posso estar errado, mas acho que é isso aí.
PS: sua resposta não está correta pois nela, o H2O2 não sofreu redução, mas sim desproporcionamento. Além disso, a reação tem de produzir ÁGUA e não hidrônio.
PS2: sim, H^+ e H3O^+ são a mesma coisa.
Espero ter lhe ajudado, Giovana. Qualquer dúvida é só perguntar!
 Re: (UNESP) Eletroquímica e Reação química
Re: (UNESP) Eletroquímica e Reação química
Muito obrigada, Christian. Resposta muito elucidativa.
Não sei se pode te ajudar, mas procurando a resposta em meu material, achei esta como a correta:
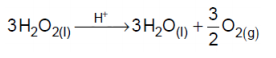
Não sei se pode te ajudar, mas procurando a resposta em meu material, achei esta como a correta:
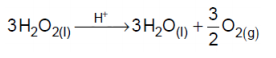

Giovana Martins- Grande Mestre

- Mensagens : 7601
Data de inscrição : 15/05/2015
Idade : 23
Localização : São Paulo
 Re: (UNESP) Eletroquímica e Reação química
Re: (UNESP) Eletroquímica e Reação química
Sim, sim. Foi essa aí que eu achei também. Mas ao pesquisar na internet em inglês achei o seguinte post:
https://www.physicsforums.com/threads/hydrogen-peroxide.77247/#post-585184
Além de mais alguns outros que afirmam que a reação de redução do peróxido de hidrogênio em meio ácido é a que citei acima.
Realmente não sei lhe afirmar qual dos dois materiais estão corretos, mas eu vou com o que postei, porque foi o que me deu na telha quando fui resolver a questão, e por achar que desproporcionamento não pode ser considerado como redução.
Boa sorte em seus estudos de química, Giovana. Tudo de bom!
https://www.physicsforums.com/threads/hydrogen-peroxide.77247/#post-585184
Além de mais alguns outros que afirmam que a reação de redução do peróxido de hidrogênio em meio ácido é a que citei acima.
Realmente não sei lhe afirmar qual dos dois materiais estão corretos, mas eu vou com o que postei, porque foi o que me deu na telha quando fui resolver a questão, e por achar que desproporcionamento não pode ser considerado como redução.
Boa sorte em seus estudos de química, Giovana. Tudo de bom!
 Re: (UNESP) Eletroquímica e Reação química
Re: (UNESP) Eletroquímica e Reação química
Ah, penso que a sua esteja correta mesmo, pois ela tem um jeito parecido com as semi-reações de redução, até na forma de expressar os 2e^-.
Novamente, muito obrigada!
Novamente, muito obrigada!

Giovana Martins- Grande Mestre

- Mensagens : 7601
Data de inscrição : 15/05/2015
Idade : 23
Localização : São Paulo
 Tópicos semelhantes
Tópicos semelhantes» |Eletroquímica| - Lei de Hess e Potencial de Reação
» Reação Química e Equação Química
» UNESP 2013- Velocidade de uma reação
» UNESP: Reação com metais + cadeia orgânica
» Estequiometria equação da reação (UNESP-2007)
» Reação Química e Equação Química
» UNESP 2013- Velocidade de uma reação
» UNESP: Reação com metais + cadeia orgânica
» Estequiometria equação da reação (UNESP-2007)
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














