entropia
2 participantes
Página 1 de 1
 entropia
entropia
um mol de gás ideal inicialmente a 25° C e 1 atm, é transformado para 40° C e 0,5 atm. Nessa transformação, são produzidos nas vizinhanças 300 J de trabalho. Se Cv,m = 3R/2, calcule ∆S.
vinsoliveira- Iniciante
- Mensagens : 13
Data de inscrição : 05/06/2012
Idade : 73
Localização : João Pessoa, PB - Brasil
 Re: entropia
Re: entropia
Clapeyron:
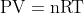
Boyle:
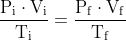
Utilizando a primeira equação temos:
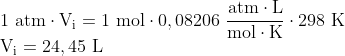
Utilizando a segunda equação:
&space;\&space;L}{298&space;\&space;K}=\dfrac{0,5&space;\&space;atm&space;\cdot&space;V_f}{313&space;\&space;K}&space;\Rightarrow&space;V_f&space;=&space;51,37&space;\&space;L})
Podemos perceber que a pressão, volume, e temperatura variam da primeira para a segunda transformação. E para resolvermos somente com esses dados, seria necessário calculo superior e integrais.
Mas temos uma maneira de resolvermos a questão:
Calculamos a variação de energia interna:
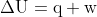
Como a temperatura aumenta, e o volume aumenta, podemos dizer que w<0 pois o sistema perde energia, e q>0, pois o sistema ganha calor.
Essa questão está meio estranha. Pelo que estou entendendo, a pressão e volume varia, e deste modo não podemos usar a capacidade calorifica do gas de volume constante.
As relações necessárias pelo exercício estão acima citadas, ou abaixo:
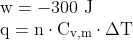
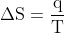
Vou procurar mais saber mais. Volto então para responder a questão.
E este tópico é de Quimica Geral e Inorgânica, movido.
Boyle:
Utilizando a primeira equação temos:
Utilizando a segunda equação:
Podemos perceber que a pressão, volume, e temperatura variam da primeira para a segunda transformação. E para resolvermos somente com esses dados, seria necessário calculo superior e integrais.
Mas temos uma maneira de resolvermos a questão:
Calculamos a variação de energia interna:
Como a temperatura aumenta, e o volume aumenta, podemos dizer que w<0 pois o sistema perde energia, e q>0, pois o sistema ganha calor.
Essa questão está meio estranha. Pelo que estou entendendo, a pressão e volume varia, e deste modo não podemos usar a capacidade calorifica do gas de volume constante.
As relações necessárias pelo exercício estão acima citadas, ou abaixo:
Vou procurar mais saber mais. Volto então para responder a questão.
E este tópico é de Quimica Geral e Inorgânica, movido.
____________________________________________
← → ↛  ⇌ ⇔ ⇐ ⇒ ⇏ ➥
⇌ ⇔ ⇐ ⇒ ⇏ ➥
 ⇌ ⇔ ⇐ ⇒ ⇏ ➥
⇌ ⇔ ⇐ ⇒ ⇏ ➥⁰ ¹ ² ³ ⁴ ⁵ ⁶ ⁷ ⁸ ⁹ ⁺ ⁻ ⁼ ⁽ ⁾ º ª ⁿ ⁱ
₀ ₁ ₂ ₃ ₄ ₅ ₆ ₇ ₈ ₉ ₊ ₋ ₌ ₍ ₎ ₐ ₑ ₒ ₓ ₔ
∴ ≈ ≠ ≡ ≢ ≤ ≥ × ± ∓ ∑ ∏ √ ∛ ∜ ∝ ∞
∀ ∃ ∈ ∉ ⊂ ⊄ ⋂ ⋃ ∧ ∨ ℝ ℕ ℚ ℤ ℂ
⊥ ║ ∡ ∠ ∢ ⊿ △ □ ▭ ◊ ○ ∆ ◦ ⊙ ⊗ ◈
Αα Ββ Γγ Δδ Εε Ζζ Ηη Θθ Ιι Κκ Λλ Μμ Νν Ξξ Οο Ππ Ρρ Σσς Ττ Υυ Φφ Χχ Ψψ Ωω ϑ ϒ ϖ ƒ ij ℓ
∫ ∬ ∭ ∳ ∂ ∇
 ℛ ℜ ℰ ℳ ℊ ℒ
ℛ ℜ ℰ ℳ ℊ ℒ
Carlos Adir- Monitor

- Mensagens : 2820
Data de inscrição : 27/08/2014
Idade : 28
Localização : Gurupi - TO - Brasil
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













