[Resolvido]Físico-química
3 participantes
Página 1 de 1
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) [Resolvido]Físico-química
[Resolvido]Físico-química
Um professor de química, em uma aula sobre ácidos e determinação do pH, resolveu diferenciar sua aula utilizando um rótulo de vinagre comercial que continha a seguinte informação:
- Concentração de ácido acético: 6,0% m/V.
Ao explicar que o vinagre é uma solução aquosa de ácido acético (ácido etanóico), o professor deixou o seguinte questionamento valendo um ponto na média: ''Qual o pH do vinagre?''
As seguintes informações foram fornecidas pelo professor:
CH3COOH: Ka ≈ 2x10-5
Massa Molar = 60g/mol
√2 ≈ 1,41; √10 ≈ 3,16 e log 4,5 ≈ 0,65
√2 ≈ 1,41; √10 ≈ 3,16 e log 4,5 ≈ 0,65
Assim, ganhará o ponto o aluno que responder que o pH é aproximadamente:
a) 1,2
b) 2,4
c) 9,6
d) 5,0
e) 7,0
a) 1,2
b) 2,4
c) 9,6
d) 5,0
e) 7,0
Última edição por velloso em Qua 01 Fev 2012, 14:09, editado 1 vez(es)

velloso- Estrela Dourada

- Mensagens : 1142
Data de inscrição : 07/04/2010
Idade : 33
Localização : Belém - Pará
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
Velloso, os dados apresentados são estes mesmos?
Consegui obter PH 3,85
Consegui obter PH 3,85
Vinícius Santana- Padawan

- Mensagens : 94
Data de inscrição : 05/06/2011
Idade : 29
Localização : Santo Amaro, Bahia, Brasil
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
Sim, Vinícius! 

velloso- Estrela Dourada

- Mensagens : 1142
Data de inscrição : 07/04/2010
Idade : 33
Localização : Belém - Pará
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
Pode ser que você esteja certo também, o valor que você encontrou é o mais próximo do gabarito...

velloso- Estrela Dourada

- Mensagens : 1142
Data de inscrição : 07/04/2010
Idade : 33
Localização : Belém - Pará
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
De boa.
Vou postar minha resolução
-----------------------------------------------------------------------------------------------------
O equilíbrio é :} + H_{2}O_{(l)}\underset{Inversa}{\overset{Direta}{\rightleftarrows}}CH_{3}COO_{(aq)}^{-}+ H_{3}O_{(aq)}^{+})
Sabemos que![[H^{+}]=\alpha M](http://latex.codecogs.com/gif.latex?[H^{+}]=\alpha M) ,
, 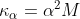 e
e ![pH= -log[H^{+}]](http://latex.codecogs.com/gif.latex?pH= -log[H^{+}])
Encontramos Alfa e depois![[H^{+}]](http://latex.codecogs.com/gif.latex?[H^{+}])
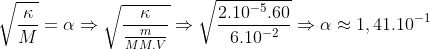
![[H^{+}]=\alpha M\Rightarrow a\frac{m}{MM V}\Rightarrow 1,41. 10^{-1}. 10^{-3}\Rightarrow 1,41.10^{-4} \frac{mol}{L}](http://latex.codecogs.com/gif.latex?[H^{+}]=\alpha M\Rightarrow a\frac{m}{MM V}\Rightarrow 1,41. 10^{-1}. 10^{-3}\Rightarrow 1,41.10^{-4} \frac{mol}{L})
E por último :
:
![pH=-log[H^{+}]\Rightarrow -log[1,41.10^{-4}]\Rightarrow pH\approx 3.85](http://latex.codecogs.com/gif.latex?pH=-log[H^{+}]\Rightarrow -log[1,41.10^{-4}]\Rightarrow pH\approx 3.85)
:afro:
Vou postar minha resolução
-----------------------------------------------------------------------------------------------------
O equilíbrio é :
Sabemos que
Encontramos Alfa e depois
E por último
:afro:
Última edição por Vinícius Santana em Ter 31 Jan 2012, 23:48, editado 1 vez(es) (Motivo da edição : Resolução Postada)
Vinícius Santana- Padawan

- Mensagens : 94
Data de inscrição : 05/06/2011
Idade : 29
Localização : Santo Amaro, Bahia, Brasil
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
Valeu Vinícius! 

velloso- Estrela Dourada

- Mensagens : 1142
Data de inscrição : 07/04/2010
Idade : 33
Localização : Belém - Pará
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
E aí, Velloso!
M = m / MM*V
M = 6 / 60*0,1
M = 1 mol/L de ácido acético
CH3COOH + H2O <===> CH3COO^- + H3O^+
Ka = [CH3COO^-]*[H3O^+] / [CH3COOH]
2*10^-5 = x*x / 1
x² = 2*10^-5
x = 4,47*10^-3 mol/L de H3O^+
pH = 3 - log 4,47
pH = 3 - 0,65
pH = 2,35
Valeu!
6% (m/V) => 6 g para 100 mL
M = m / MM*V
M = 6 / 60*0,1
M = 1 mol/L de ácido acético
CH3COOH + H2O <===> CH3COO^- + H3O^+
Ka = [CH3COO^-]*[H3O^+] / [CH3COOH]
2*10^-5 = x*x / 1
x² = 2*10^-5
x = 4,47*10^-3 mol/L de H3O^+
pH = 3 - log 4,47
pH = 3 - 0,65
pH = 2,35
Valeu!
Luís- Estrela Dourada

- Mensagens : 1177
Data de inscrição : 09/02/2011
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
Luís escreveu:E aí, Velloso!6% (m/V) => 6 g para 100 mL
M = m / MM*V
M = 6 / 60*0,1
M = 1 mol/L de ácido acético
CH3COOH + H2O <===> CH3COO^- + H3O^+
Ka = [CH3COO^-]*[H3O^+] / [CH3COOH]
2*10^-5 = x*x / 1
x² = 2*10^-5
x = 4,47*10^-3 mol/L de H3O^+
pH = 3 - log 4,47
pH = 3 - 0,65
pH = 2,35
Valeu!
Tá explicado
:afro:
Vinícius Santana- Padawan

- Mensagens : 94
Data de inscrição : 05/06/2011
Idade : 29
Localização : Santo Amaro, Bahia, Brasil
![[Resolvido]Físico-química Empty](https://2img.net/i/empty.gif) Re: [Resolvido]Físico-química
Re: [Resolvido]Físico-química
Show de bola, Luís. Muito obrigado meu amigo! 

velloso- Estrela Dourada

- Mensagens : 1142
Data de inscrição : 07/04/2010
Idade : 33
Localização : Belém - Pará
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|


![[Resolvido]Físico-química T3Ri1xW](https://i.imgur.com/T3Ri1xW.png)










