Soluções
2 participantes
Página 1 de 1
 Soluções
Soluções
Foram misturados 100 mL de solução aquosa 0,4 mol/L de ácido clorídrico, com 100 mL de solução de hidróxido de cálcio, de mesma concentração.
a) Ao final da reação, o meio ficará ácido ou básico? Justifique sua resposta com cálculos.
b) Calcule a concentração molar do reagente remanescente na mistura.
a) Ao final da reação, o meio ficará ácido ou básico? Justifique sua resposta com cálculos.
b) Calcule a concentração molar do reagente remanescente na mistura.
juslopessss- Iniciante
- Mensagens : 15
Data de inscrição : 23/03/2022
 Re: Soluções
Re: Soluções
Olá Juslopes;
O ácido clorídrico reage da seguinte forma com o hidróxido de cálcio:

Perceba que o ácido clorídrico e o hidróxido de cálcio estão na proporção 2:1, isso significa que a cada 2 mols de HCl precisamos de 1 mol de Ba(OH)2, sem essa proporção os dois não reagem. Vamos calcular a quantidade de matéria de cada espécie, utilizando a informação de concentração, assim:
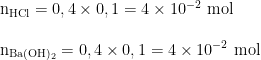
Esses se encontram na proporção 1:1, dessa forma, todo o ácido é consumido, restando ainda 2 x 10⁻² mol de hidróxido de bário. Portanto, o meio ficará básico.
Calculo da concentração molar remanescente:
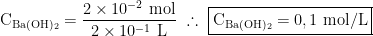
Tem o gabarito?
O ácido clorídrico reage da seguinte forma com o hidróxido de cálcio:
Perceba que o ácido clorídrico e o hidróxido de cálcio estão na proporção 2:1, isso significa que a cada 2 mols de HCl precisamos de 1 mol de Ba(OH)2, sem essa proporção os dois não reagem. Vamos calcular a quantidade de matéria de cada espécie, utilizando a informação de concentração, assim:
Esses se encontram na proporção 1:1, dessa forma, todo o ácido é consumido, restando ainda 2 x 10⁻² mol de hidróxido de bário. Portanto, o meio ficará básico.
Calculo da concentração molar remanescente:
Tem o gabarito?

qedpetrich- Monitor

- Mensagens : 2495
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













