estequiometria com pureza e rendimento
2 participantes
Página 1 de 1
 estequiometria com pureza e rendimento
estequiometria com pureza e rendimento
[list=23]
[*]Em um laboratório de Química uma aluna colocou em um Becker 100 g de calcário e excesso de ácido clorídrico. Considerando o grau de pureza do carbonato de cálcio no calcário igual a 80%, em uma temperatura de 27 oC e 2 atm de pressão, admitindo-se um rendimento de 90% na reação, o volume de gás liberado, aproximado, é:
a) 9,84 L
b) 8,85 L
c) 12,3 L
d) 11,07 L
[/list]
[*]Em um laboratório de Química uma aluna colocou em um Becker 100 g de calcário e excesso de ácido clorídrico. Considerando o grau de pureza do carbonato de cálcio no calcário igual a 80%, em uma temperatura de 27 oC e 2 atm de pressão, admitindo-se um rendimento de 90% na reação, o volume de gás liberado, aproximado, é:
a) 9,84 L
b) 8,85 L
c) 12,3 L
d) 11,07 L
[/list]
mariaclara23@med- Iniciante
- Mensagens : 25
Data de inscrição : 26/11/2018
Idade : 22
Localização : mossoro, RN, brasil
 Re: estequiometria com pureza e rendimento
Re: estequiometria com pureza e rendimento
Reação: 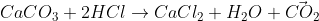
[80% | PUREZA] Como ele colocou 100 gramas para reagir, porém ,somente, 80 gramas irão de fato servir para a reação, pois os outros 20% é composto por impurezas que não irão reagir
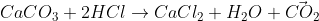
100g/mol 73g/mol
73g/mol 111g/mol
111g/mol 18g/mol
18g/mol 44g/mol
44g/mol
[ESTEQUIOMETRIA| RENDIMENTO 90%] Como o HCl está em excesso ; iremos, usar a proporção recomentada de CaCO3 para achar a o número de mols de gás produzido, usando a Equação de Clapeyron para gases ideais:
100g/mol (CaCO3) 1mol(CO2)
1mol(CO2)
80g

 =0,8 mols | Isso para um rendimento de 100%
=0,8 mols | Isso para um rendimento de 100%
Logo, para um rendimento de 90%
 =0,72mols
=0,72mols
[VOLUME DE GASES IDEAIS]
P=2 atm
V= ?
 =0,72mol
=0,72mol
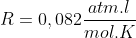
Usando essas relações, você chegará a: =8,85 litros
=8,85 litros
[80% | PUREZA] Como ele colocou 100 gramas para reagir, porém ,somente, 80 gramas irão de fato servir para a reação, pois os outros 20% é composto por impurezas que não irão reagir
100g/mol
[ESTEQUIOMETRIA| RENDIMENTO 90%] Como o HCl está em excesso ; iremos, usar a proporção recomentada de CaCO3 para achar a o número de mols de gás produzido, usando a Equação de Clapeyron para gases ideais:
100g/mol (CaCO3)
80g
Logo, para um rendimento de 90%
[VOLUME DE GASES IDEAIS]
P=2 atm
V= ?
Usando essas relações, você chegará a:

Unßer- Padawan

- Mensagens : 82
Data de inscrição : 09/02/2017
Idade : 25
Localização : Juazeiro,Bahia
 Tópicos semelhantes
Tópicos semelhantes» Pureza e rendimento de uma reação.
» Estequiometria (Pureza)
» Estequiometria rendimento e excesso
» Estequiometria envolvendo rendimento
» Estequiometria - Rendimento
» Estequiometria (Pureza)
» Estequiometria rendimento e excesso
» Estequiometria envolvendo rendimento
» Estequiometria - Rendimento
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













