Pressão Parcial do Hidrogênio
2 participantes
Página 1 de 1
 Pressão Parcial do Hidrogênio
Pressão Parcial do Hidrogênio
Considere a corrosão de um pedaço de palhinha de aço por ácido clorídrico, com a produção de 80 mL de  e vapor d'água, que é recolhido e mensurado numa proveta, conforme mostra a figura. A pressão do vapor de água, na temperatura do experimento, 27 °C, é de cerca de 0,04 atm. A pressão loca é 1 atm.
e vapor d'água, que é recolhido e mensurado numa proveta, conforme mostra a figura. A pressão do vapor de água, na temperatura do experimento, 27 °C, é de cerca de 0,04 atm. A pressão loca é 1 atm.

Qual é a pressão parcial do hidrogênio produzido?
Gabarito:
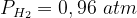

Qual é a pressão parcial do hidrogênio produzido?
Gabarito:

Adam Zunoeta- Monitor

- Mensagens : 4223
Data de inscrição : 25/08/2010
Idade : 34
Localização : Cuiabá
 Re: Pressão Parcial do Hidrogênio
Re: Pressão Parcial do Hidrogênio
Eu vou transcrever um trecho do meu livro sobre esse assunto de pressão parcial:
Quando dois ou mais gases que não reagem quimicamente são colocados num mesmo reservatório, a pressão exercida por cada gás na mistura é a mesma que ele teria se estivesse sozinho no reservatório. A pressão exercida por cada gás em uma mistura é chamada de pressão parcial e, como foi observado por John Dalton, a pressão total é igual à soma das pressões parciais de cada gás, na mistura:
Pt = pa + pb + pc + ...
onde Pt é a pressão total da mistura e pa, pb e pc são as pressões parciais dos gases a, b e c, respectivamente.
Os gases preparados no laboratório são, muito frequentemente, coletados por deslocamento de água. Um gás coletado dessa maneira torna-se "contaminado" com moléculas de água que evaporam do gás. Essas moléculas de água também exercem uma pressão chamada pressão de vapor.
A pressão de vapor da água contribui para a pressão total do gás "úmido":
Pt = pgás + pH2O
Usando essa equação com os dados do exercício:
1 = pgás + 0,04
pgás = 0,96 atm
Abraço!!
P.S.: Eu ainda não vi Lost Canvas, mas pretendo.
Sobre os gráficos, acontece que eles querem fazer os mais perfeitos possíveis e às vezes perde mesmo a originalidade.
Qual foi sua saga preferida?
Quando dois ou mais gases que não reagem quimicamente são colocados num mesmo reservatório, a pressão exercida por cada gás na mistura é a mesma que ele teria se estivesse sozinho no reservatório. A pressão exercida por cada gás em uma mistura é chamada de pressão parcial e, como foi observado por John Dalton, a pressão total é igual à soma das pressões parciais de cada gás, na mistura:
Pt = pa + pb + pc + ...
onde Pt é a pressão total da mistura e pa, pb e pc são as pressões parciais dos gases a, b e c, respectivamente.
Os gases preparados no laboratório são, muito frequentemente, coletados por deslocamento de água. Um gás coletado dessa maneira torna-se "contaminado" com moléculas de água que evaporam do gás. Essas moléculas de água também exercem uma pressão chamada pressão de vapor.
A pressão de vapor da água contribui para a pressão total do gás "úmido":
Pt = pgás + pH2O
Usando essa equação com os dados do exercício:
1 = pgás + 0,04
pgás = 0,96 atm
Abraço!!
P.S.: Eu ainda não vi Lost Canvas, mas pretendo.
Sobre os gráficos, acontece que eles querem fazer os mais perfeitos possíveis e às vezes perde mesmo a originalidade.
Qual foi sua saga preferida?
Luís- Estrela Dourada

- Mensagens : 1177
Data de inscrição : 09/02/2011
 Re: Pressão Parcial do Hidrogênio
Re: Pressão Parcial do Hidrogênio
Show a resposta Luís !
P.S.: Eu ainda não vi Lost Canvas, mas pretendo.
Sobre os gráficos, acontece que eles querem fazer os mais perfeitos possíveis e às vezes perde mesmo a originalidade.
Qual foi sua saga preferida?
A saga de Hades , principalmente a parte dos elíseos (ela podia ter sido um pouco maior ). :
). :
P.S.: Eu ainda não vi Lost Canvas, mas pretendo.
Sobre os gráficos, acontece que eles querem fazer os mais perfeitos possíveis e às vezes perde mesmo a originalidade.
Qual foi sua saga preferida?
A saga de Hades , principalmente a parte dos elíseos (ela podia ter sido um pouco maior

Adam Zunoeta- Monitor

- Mensagens : 4223
Data de inscrição : 25/08/2010
Idade : 34
Localização : Cuiabá
 Tópicos semelhantes
Tópicos semelhantes» ITA - Comportamento da relação densidade/pressão em função da pressão do gás hidrogênio
» Pressão parcial
» Pressão Parcial
» Pressão Parcial
» Pressão parcial
» Pressão parcial
» Pressão Parcial
» Pressão Parcial
» Pressão parcial
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













