Propriedades Periódicas
2 participantes
Página 1 de 1
 Propriedades Periódicas
Propriedades Periódicas
(Fuvest-SP) O gráfico mostra a variação do potencial de ionização para elementos com número atômico (Z) de 1 a 19.
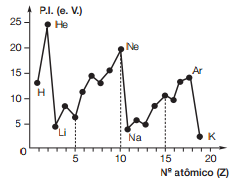
a) Dê o nome dos três elementos que têm maior dificuldade de formar cátions, no estado gasoso.
b) Explique por que, no intervalo de Z = 3 a Z = 10, o potencial de ionização tende a crescer com o aumento do número atômico.

a) Dê o nome dos três elementos que têm maior dificuldade de formar cátions, no estado gasoso.
b) Explique por que, no intervalo de Z = 3 a Z = 10, o potencial de ionização tende a crescer com o aumento do número atômico.
Matheus Vasconcelos- Padawan

- Mensagens : 78
Data de inscrição : 16/09/2014
Idade : 25
Localização : Fortaleza
 Re: Propriedades Periódicas
Re: Propriedades Periódicas
a) Apresentará dificuldade em forma cátions aqueles que apresentam um alto potencial de ionização. Logo, são eles: Hélio, Neônio e Argônio.
b) Repare que de Z=3 à Z=10 todos os elementos pertencem a terceira linha da Tabela Periódica. Logo, todos eles possuem o mesmo número de níveis. Dessa forma, o aumento do número atômico irá aumentar a força de atração eletrostática entre próton-elétron, necessitando de maior energia para superar essa mesma força para "arrancar" o elétron.
b) Repare que de Z=3 à Z=10 todos os elementos pertencem a terceira linha da Tabela Periódica. Logo, todos eles possuem o mesmo número de níveis. Dessa forma, o aumento do número atômico irá aumentar a força de atração eletrostática entre próton-elétron, necessitando de maior energia para superar essa mesma força para "arrancar" o elétron.

saulocoaster- Recebeu o sabre de luz

- Mensagens : 121
Data de inscrição : 31/05/2013
Idade : 26
Localização : Salvador
 Re: Propriedades Periódicas
Re: Propriedades Periódicas
saulocoaster escreveu:a) Apresentará dificuldade em forma cátions aqueles que apresentam um alto potencial de ionização. Logo, são eles: Hélio, Neônio e Argônio.
b) Repare que de Z=3 à Z=10 todos os elementos pertencem a terceira linha da Tabela Periódica. Logo, todos eles possuem o mesmo número de níveis. Dessa forma, o aumento do número atômico irá aumentar a força de atração eletrostática entre próton-elétron, necessitando de maior energia para superar essa mesma força para "arrancar" o elétron.
Só mais uma dúvida, o elemento com Z=9 não teria maior potencial de ionização que o Argônio ?
Matheus Vasconcelos- Padawan

- Mensagens : 78
Data de inscrição : 16/09/2014
Idade : 25
Localização : Fortaleza
 Re: Propriedades Periódicas
Re: Propriedades Periódicas
É verdade. Acabei me passando nisso. Logo seria Hélio, Neônio e Flúor.

saulocoaster- Recebeu o sabre de luz

- Mensagens : 121
Data de inscrição : 31/05/2013
Idade : 26
Localização : Salvador
 Tópicos semelhantes
Tópicos semelhantes» propriedades periódicas
» Propriedades Periódicas
» PROPRIEDADES PERIÓDICAS
» Propriedades Periódicas
» Propriedades Periódicas
» Propriedades Periódicas
» PROPRIEDADES PERIÓDICAS
» Propriedades Periódicas
» Propriedades Periódicas
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













