(ITA) Estequiometria
5 participantes
Página 1 de 1
 (ITA) Estequiometria
(ITA) Estequiometria
Um método de obtenção de prata pura e porosa consiste na decomposição térmica de seu carbonato. Qual massa de prata seria obtida pela decomposição de um quilograma de 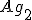 C
C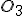 ?
?
a) (1000 g / 275,8 g) x 107,9 g
b) (1000 g / 275,8 g / mol) x 215,8 g / mol
c) (275,8 g / 107,9 g / mol) x 1000 g / mol
d) (1000 g / 215,8 g / mol) x 275,8 g
e) (275,8 g / 1000 g) x 107,8 mol
Como devo proceder para chegar em tal resposta (em negrito), desde a montagem da reação de decomposição inical?
Grato desde já.
Obs.: tenho a resposta toda formulada, se ajudar, posso postá-la.
a) (1000 g / 275,8 g) x 107,9 g
b) (1000 g / 275,8 g / mol) x 215,8 g / mol
c) (275,8 g / 107,9 g / mol) x 1000 g / mol
d) (1000 g / 215,8 g / mol) x 275,8 g
e) (275,8 g / 1000 g) x 107,8 mol
Como devo proceder para chegar em tal resposta (em negrito), desde a montagem da reação de decomposição inical?
Grato desde já.
Obs.: tenho a resposta toda formulada, se ajudar, posso postá-la.
____________________________________________
"Death is so terribly final, while life is full of possibilities." - Tyrion Lannister
 Re: (ITA) Estequiometria
Re: (ITA) Estequiometria
1 Ag2CO3(s) -----> 2 Ag(s) + 1 CO2(g) + 1/2 O2(g)
Massa molar (Ag2CO3) = 2.(107,9) + 12 + 3(16) = 275,8 g/mol
Temos um quilo de Ag2CO3, e em cada mol dele teremos dois mols de Ag, logo, a massa de prata será:
m = (1000 g de Ag2CO3)*(1 mol de Ag2CO3/275,8 g de Ag2CO3)*(2*107,9 g de Ag2CO3/1 mol de Ag2CO3)
m = (1000 g / 275,8 g / mol) x 215,8 g / mol
Massa molar (Ag2CO3) = 2.(107,9) + 12 + 3(16) = 275,8 g/mol
Temos um quilo de Ag2CO3, e em cada mol dele teremos dois mols de Ag, logo, a massa de prata será:
m = (1000 g de Ag2CO3)*(1 mol de Ag2CO3/275,8 g de Ag2CO3)*(2*107,9 g de Ag2CO3/1 mol de Ag2CO3)
m = (1000 g / 275,8 g / mol) x 215,8 g / mol

Matheus Bertolino- Fera

- Mensagens : 941
Data de inscrição : 10/08/2011
Idade : 27
Localização : Goioerê, Paraná, Brasil
 Re: (ITA) Estequiometria
Re: (ITA) Estequiometria
Achei estranha essa resposta. A massa molar de Ag é 107,9. Portanto a o valor 215,8 tem unidade mols.g/mol = g

jpspindola- Padawan

- Mensagens : 55
Data de inscrição : 27/03/2015
Idade : 26
Localização : Rio de Janeiro
 Re: (ITA) Estequiometria
Re: (ITA) Estequiometria
Ag2CO3 ---> 2Ag +CO2 + 1/2O2
Ag2CO3 = 276g/mol.
2Ag = 216g/mol
276----216
1000------x
x = 782,6.
Resolvendo as equações das alternativas apresentadas, a única que bate a resposta é a B.
Resposta por tentativa e erro, mas isto não tira o mérito.
Ag2CO3 = 276g/mol.
2Ag = 216g/mol
276----216
1000------x
x = 782,6.
Resolvendo as equações das alternativas apresentadas, a única que bate a resposta é a B.
Resposta por tentativa e erro, mas isto não tira o mérito.
 Re: (ITA) Estequiometria
Re: (ITA) Estequiometria
Chries, a resolução não se dá por tentativa e erro.
m_{Ag}=\frac{2\cdot 107,9 \cdot 1000}{275,8} \iff \boxed{m_{Ag}=\frac{1000 \cdot 215,8}{275,8}}}
O que corresponde à alternativa B.
O que corresponde à alternativa B.
Mimetist- Matador

- Mensagens : 460
Data de inscrição : 14/03/2015
Idade : 31
Localização : São Paulo
 Re: (ITA) Estequiometria
Re: (ITA) Estequiometria
Sim, eu sei. Não foi isso que eu quis dizer, Mimetist.
O que eu quis dizer é que a minha forma de responder a questão foi por tentativa e erro, não que não existem formas de responder sem utilizá-la.
O que eu quis dizer é que a minha forma de responder a questão foi por tentativa e erro, não que não existem formas de responder sem utilizá-la.
 Re: (ITA) Estequiometria
Re: (ITA) Estequiometria
Ah, entendi, Chries!
Assim sendo, há duas formas de resolução a mais, haha.
Assim sendo, há duas formas de resolução a mais, haha.

Mimetist- Matador

- Mensagens : 460
Data de inscrição : 14/03/2015
Idade : 31
Localização : São Paulo
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|















