Orgânica
3 participantes
PiR2 :: Química :: Química Orgânica
Página 1 de 1
 Orgânica
Orgânica
28. (UFRGS 2017) O Prêmio Nobel de Química de 2016 foi concedido aos
cientistas Jean-Pierre Sauvage, Sir J. Fraser Stoddart e Bernard L. Feringa que
desenvolveram máquinas moleculares. Essas moléculas, em função de estímulos
externos, realizam movimentos controlados que poderão levar, no futuro, à execução de tarefas de uma máquina na escala nanométrica (10-9 m). Abaixo está mostrada uma molécula na qual, pela
irradiação de luz (fotoestimulação), o isômero A é convertido no isômero B. Sob aquecimento (termoestimulação), o
isômero B novamente se converte no isômero A.
A respeito disso, considere as seguintes afirmações.
I - A e B são isômeros geométricos em que os substituintes na ligação N=N estão em lados opostos no isômero A e, no
mesmo lado, no isômero B.
II - A interação do grupo – +NH3 com o heterociclo, no isômero B, é do tipo ligação de hidrogênio.
III- Todos os nitrogênios presentes nos dois isômeros apresentam uma estrutura tetraédrica.
Quais estão corretas?
A) Apenas I. B) Apenas III. C) Apenas I e II. D) Apenas II e III. E) I, II e III.
GAB: C
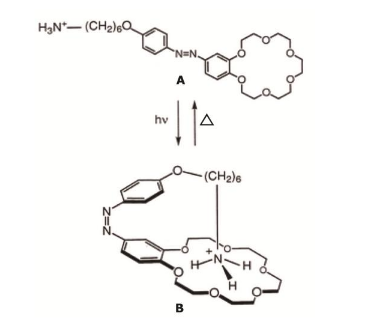
Minha dúvida é na afirmação 2: Por que a interação do NH3 com o ciclo é do O que se liga ao H, e não do C que se liga ao H?
Pois eu pensei que o oxigênio já estaria estável com aquelas duas ligações, não podendo realizar uma terceira. Se fosse do C com o H a resposta não seria ligações de hidrogênio
Achei essa imagem na internet, que mostra as ligações do O com o H
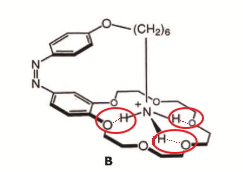
Obrigado
cientistas Jean-Pierre Sauvage, Sir J. Fraser Stoddart e Bernard L. Feringa que
desenvolveram máquinas moleculares. Essas moléculas, em função de estímulos
externos, realizam movimentos controlados que poderão levar, no futuro, à execução de tarefas de uma máquina na escala nanométrica (10-9 m). Abaixo está mostrada uma molécula na qual, pela
irradiação de luz (fotoestimulação), o isômero A é convertido no isômero B. Sob aquecimento (termoestimulação), o
isômero B novamente se converte no isômero A.
A respeito disso, considere as seguintes afirmações.
I - A e B são isômeros geométricos em que os substituintes na ligação N=N estão em lados opostos no isômero A e, no
mesmo lado, no isômero B.
II - A interação do grupo – +NH3 com o heterociclo, no isômero B, é do tipo ligação de hidrogênio.
III- Todos os nitrogênios presentes nos dois isômeros apresentam uma estrutura tetraédrica.
Quais estão corretas?
A) Apenas I. B) Apenas III. C) Apenas I e II. D) Apenas II e III. E) I, II e III.
GAB: C

Minha dúvida é na afirmação 2: Por que a interação do NH3 com o ciclo é do O que se liga ao H, e não do C que se liga ao H?
Pois eu pensei que o oxigênio já estaria estável com aquelas duas ligações, não podendo realizar uma terceira. Se fosse do C com o H a resposta não seria ligações de hidrogênio
Achei essa imagem na internet, que mostra as ligações do O com o H

Obrigado
Enzo _Sergi- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 30/07/2020
Idade : 21
Localização : Porto Alegre, RS, Brasil
 Re: Orgânica
Re: Orgânica
Exato, mas entre a molécula dos H's da Molécula de NH3 e o O's são interações intermoleculares e são conhecidas, erroneamente, como pontes de hidrogênio. O jeito correto é "Ligação de Hidrogênio".
As ligações covalentes existentes entre os Carbonos e os Oxigênios da molécula maior são interações intramoleculares.
Portanto, as ligações de Hidrogênio citadas no texto são interações intermoleculares e só ocorrem entre Hidrogênio-Flúor,Oxigênio e Nitrogênio
Espero ter ajudado!Abraços!
As ligações covalentes existentes entre os Carbonos e os Oxigênios da molécula maior são interações intramoleculares.
Portanto, as ligações de Hidrogênio citadas no texto são interações intermoleculares e só ocorrem entre Hidrogênio-Flúor,Oxigênio e Nitrogênio
Espero ter ajudado!Abraços!
Última edição por FocoNoITA em Ter 01 Set 2020, 17:00, editado 2 vez(es)

FocoNoIMEITA- Jedi

- Mensagens : 270
Data de inscrição : 05/05/2020
Idade : 21
Localização : Rio de Janeiro-RJ
 Re: Orgânica
Re: Orgânica
FocoNoITA escreveu:Exato, mas entre a molécula dos H's da Molécula de NH3 e o O's são ligações intermoleculares e são conhecidas, erroneamente, como pontes de hidrogênio. O jeito correto é Ligação de Hidrogênio.
As ligações covalentes existentes entre os Carbonos e os Oxigênios da molécula maior são ligações intramoleculares.
Portanto, as ligações de Hidrogênio citadas no texto são ligações intermoleculares e só ocorrem entre Hidrogênio-Flúor,Oxigênio e Nitrogênio
Espero ter ajudado!Abraços!
Obrigado pela resposta!
Mas eu ainda fiquei com uma dúvida.... como os Oxigênios do ciclo iriam realizar as ligações de hidrogênio com os Hidrogênios, sendo que os oxigênios já estão com duas ligações e não aceitam octeto expandido?
Por isso que eu pensei que fossem os Carbonos do ciclo realizando ligações com os Hidrogênios do NH3, pois sem essas ligações os carbonos ficariam com ligações a fazer. Se fosse assim a interação do ciclo com o NH3 não seria ligação de H, como a alternativa indica
Enzo _Sergi- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 30/07/2020
Idade : 21
Localização : Porto Alegre, RS, Brasil
 Re: Orgânica
Re: Orgânica
Boa noite!
A interação ocorre com o oxigênio porque ele é mais eletronegativo que o carbono, assim, atrai os elétrons mais "fortemente".
O oxigênio não tem seu octeto expandido, o que está ocorrendo é uma atração que acaba contraindo essa parte da molécula. Isso também pode ocorrer porque há um efeito indutivo no oxigênio que não há resultante nula, por conta dos vetores (observe que o oxigênio está numa geometria angular). Pela molécula, também percebemos que a quantidade de oxigênio não é proporcional a de hidrogênio, o que também garante que a atração não terá resultante nula (assim, criando uma "indução" polar) e criando ligações de hidrogênio.
O que está ocorrendo é mais uma atração, não necessariamente uma ligação, formação e quebra de moléculas...
Lembre-se também que estudamos apenas a teoria, na prática é outra história! Então é sempre bom pensar um pouco além do que aquilo que lemos em livros. Espero ter ajudado!!!
A interação ocorre com o oxigênio porque ele é mais eletronegativo que o carbono, assim, atrai os elétrons mais "fortemente".
O oxigênio não tem seu octeto expandido, o que está ocorrendo é uma atração que acaba contraindo essa parte da molécula. Isso também pode ocorrer porque há um efeito indutivo no oxigênio que não há resultante nula, por conta dos vetores (observe que o oxigênio está numa geometria angular). Pela molécula, também percebemos que a quantidade de oxigênio não é proporcional a de hidrogênio, o que também garante que a atração não terá resultante nula (assim, criando uma "indução" polar) e criando ligações de hidrogênio.
O que está ocorrendo é mais uma atração, não necessariamente uma ligação, formação e quebra de moléculas...
Lembre-se também que estudamos apenas a teoria, na prática é outra história! Então é sempre bom pensar um pouco além do que aquilo que lemos em livros. Espero ter ajudado!!!
niett- Iniciante
- Mensagens : 16
Data de inscrição : 21/06/2020
PiR2 :: Química :: Química Orgânica
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













