Estequiometria (dúvida)
3 participantes
Página 1 de 1
 Estequiometria (dúvida)
Estequiometria (dúvida)
Num processo de obtenção de ferro a partir da hematita (Fe2O3), considere a equação não balanceada:
Fe2O3 + C ---> Fe + CO
Utilizando-se 4,8 toneladas de minério e admitindo-se um rendimento de 80% na reação, a quantidade de ferro produzida será de: Pesos atômicos: C = 12; O = 16; Fe = 56
a) 2688 kg
b) 3360 kg
c) 1344 t
d) 2688 t
e) 3360 t
Prezados, a resolução para chegar na resposta é apenas uma regra de três considerando a massa disponível, os coeficientes estequimétricos e o rendimento. Contudo, realizei de outra forma (abaixo) e gostaria de saber onde eu errei.
16.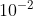 (F2O3) --------1 mol
(F2O3) --------1 mol
48.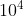 -------- 3.
-------- 3.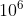 mol
mol
Balanceamento >>> Fe2O3 + 3C ---> 2Fe + 3CO
Portanto, 3.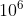 mols de F2O3 corresponde a 6.
mols de F2O3 corresponde a 6.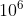 mols de Fe. Assim : 6.
mols de Fe. Assim : 6.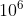 . 54.
. 54.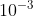 = 324.
= 324. 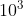 kg. Aqui já fica estranho, como eu teria 324 toneladas de Fe??? Enfim, se continuar com a lógica, fica > 324.
kg. Aqui já fica estranho, como eu teria 324 toneladas de Fe??? Enfim, se continuar com a lógica, fica > 324. 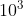 kg . 0,8 >> 259,2.
kg . 0,8 >> 259,2.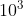 kg
kg
Preciso entender por que essa conta não funciona. O rendimento de 80% deve ser proporcional às massas dos produtos? Não posso considerar essa relação entre o coeficiente estequiométrico do F2O3 e F??
Desde já agradeço
Fe2O3 + C ---> Fe + CO
Utilizando-se 4,8 toneladas de minério e admitindo-se um rendimento de 80% na reação, a quantidade de ferro produzida será de: Pesos atômicos: C = 12; O = 16; Fe = 56
a) 2688 kg
b) 3360 kg
c) 1344 t
d) 2688 t
e) 3360 t
Prezados, a resolução para chegar na resposta é apenas uma regra de três considerando a massa disponível, os coeficientes estequimétricos e o rendimento. Contudo, realizei de outra forma (abaixo) e gostaria de saber onde eu errei.
16.
48.
Balanceamento >>> Fe2O3 + 3C ---> 2Fe + 3CO
Portanto, 3.
Preciso entender por que essa conta não funciona. O rendimento de 80% deve ser proporcional às massas dos produtos? Não posso considerar essa relação entre o coeficiente estequiométrico do F2O3 e F??
Desde já agradeço
Última edição por PedroFagundes em Qua 02 Set 2020, 20:50, editado 2 vez(es)
PedroFagundes- Recebeu o sabre de luz

- Mensagens : 128
Data de inscrição : 27/07/2020
 Re: Estequiometria (dúvida)
Re: Estequiometria (dúvida)
Pra ser sincero eu não entendi a sua resolução.
Veja como eu fiz.
Fe2O3 + 3C ---> 2Fe + 3CO
160g de Fe2O3 ---- 2x56g de Fe
4,8.10^6g de Fe2O3 ---- x(g) de Fe
x=3,36t de Fe (Se o rendimento fosse de 100%)
A quantidade real (x') de Ferro produzida é: x'=x.R, R=Rendimento da reação
x'=3,36t x 0,80
x'=2,688t = 2688kg de Fe
Veja como eu fiz.
Fe2O3 + 3C ---> 2Fe + 3CO
160g de Fe2O3 ---- 2x56g de Fe
4,8.10^6g de Fe2O3 ---- x(g) de Fe
x=3,36t de Fe (Se o rendimento fosse de 100%)
A quantidade real (x') de Ferro produzida é: x'=x.R, R=Rendimento da reação
x'=3,36t x 0,80
x'=2,688t = 2688kg de Fe

marcosprb- Mestre Jedi

- Mensagens : 825
Data de inscrição : 08/05/2017
 Re: Estequiometria (dúvida)
Re: Estequiometria (dúvida)
Como o marcosprb não entendeu, acredito que alguém pode não ter entendido também. Como eu entendi e eu também gostaria de saber onde está o erro, colocarei o cálculo detalhado:
x = n° de mol em 4,8 t de Fe2O3
y = n° de mol de Fe em x de Fe2O3
z = quantos kg tem y mol
w = resultado final
\begin{gather*}
16.10^{-2} \ kg\ ---\ 1\ mol\\
48.10^{4} kg\ ---\ x\\
\\
x\ =\ 3.10^{6} \ mol\\
\\
1\ mol\ ---\ 2\ mol\\
3.10^{6} \ mol\ ---\ y\\
\\
y\ =\ 6.10^{6} \ mol\\
\\
1\ mol\ ---\ 54.10^{-3} \ kg\\
6.10^{6} \ mol\ ---\ z\\
\\
z\ =\ 324.10^{3} \ kg\\
\\
w\ =\ 324.10^{3} \ *\ 0,8\ \Longrightarrow \ w\ =\ 259,2.10^{3} \ kg
\end{gather*}
x = n° de mol em 4,8 t de Fe2O3
y = n° de mol de Fe em x de Fe2O3
z = quantos kg tem y mol
w = resultado final
\begin{gather*}
16.10^{-2} \ kg\ ---\ 1\ mol\\
48.10^{4} kg\ ---\ x\\
\\
x\ =\ 3.10^{6} \ mol\\
\\
1\ mol\ ---\ 2\ mol\\
3.10^{6} \ mol\ ---\ y\\
\\
y\ =\ 6.10^{6} \ mol\\
\\
1\ mol\ ---\ 54.10^{-3} \ kg\\
6.10^{6} \ mol\ ---\ z\\
\\
z\ =\ 324.10^{3} \ kg\\
\\
w\ =\ 324.10^{3} \ *\ 0,8\ \Longrightarrow \ w\ =\ 259,2.10^{3} \ kg
\end{gather*}
EternoEstudante- Iniciante
- Mensagens : 36
Data de inscrição : 04/11/2019
Idade : 24
Localização : Brasil
PedroFagundes gosta desta mensagem
 Re: Estequiometria (dúvida)
Re: Estequiometria (dúvida)
Agradeço a sua resolução Marcos e também agradeço ao Eterno Estudante por deixar de maneira mais clara.
A dúvida continua...
A dúvida continua...
PedroFagundes- Recebeu o sabre de luz

- Mensagens : 128
Data de inscrição : 27/07/2020
 Re: Estequiometria (dúvida)
Re: Estequiometria (dúvida)
Eterno Estudante, poxa vida. Errei feio, errei rude.
Ocorre que a resolução já começou errada lá na notação, e extrapola no número de massa de 1 mol de Fe que é 56 e não 54! Enfim, fica que:
Relação de Fe2O3 para 2Fe é 1:2
1 mol Fe2O3 ----- 160g ou 0,16kg
x mol Fe2O3 ----- 48.10^5g
x = 3.10^4 mol
Considerando a relação de 1:2, temos de Fe terá 6.10^4 mol
6.10^4 mol * 56.10^-3 kg * 0,8 = 2688 kg de Fe
Erro aritmético é sempre uma vergonha. Peço desculpa a todos.
Ocorre que a resolução já começou errada lá na notação, e extrapola no número de massa de 1 mol de Fe que é 56 e não 54! Enfim, fica que:
Relação de Fe2O3 para 2Fe é 1:2
1 mol Fe2O3 ----- 160g ou 0,16kg
x mol Fe2O3 ----- 48.10^5g
x = 3.10^4 mol
Considerando a relação de 1:2, temos de Fe terá 6.10^4 mol
6.10^4 mol * 56.10^-3 kg * 0,8 = 2688 kg de Fe
Erro aritmético é sempre uma vergonha. Peço desculpa a todos.
PedroFagundes- Recebeu o sabre de luz

- Mensagens : 128
Data de inscrição : 27/07/2020
EternoEstudante gosta desta mensagem
 Re: Estequiometria (dúvida)
Re: Estequiometria (dúvida)
Realmente, erros básicos. Mas você acredita que eu resolvi a questão para te responder (pois eu achava uma questão fácil e eu realmente acertei o gabarito), mas quando vi a tua resolução eu não consegui achar o erro? Bom, já era madrugada, eu estava bem cansado e nem prestei atenção nisso que você citou. Mas acontece, não é mesmo?
Acho que você não deve pedir desculpas e nem ficar cabisbaixo. Todos nós erramos e aprendemos todos dias. Obrigado por retornar com a solução, pois eu não havia entendido o porquê de o cálculo estar errado até hoje, embora eu não tenha tentado novamente essa questão utilizando os mesmos caminhos que você tentou utilizar.
Acho que você não deve pedir desculpas e nem ficar cabisbaixo. Todos nós erramos e aprendemos todos dias. Obrigado por retornar com a solução, pois eu não havia entendido o porquê de o cálculo estar errado até hoje, embora eu não tenha tentado novamente essa questão utilizando os mesmos caminhos que você tentou utilizar.
EternoEstudante- Iniciante
- Mensagens : 36
Data de inscrição : 04/11/2019
Idade : 24
Localização : Brasil
PedroFagundes gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» Dúvida estequiometria
» Estequiometria - Dúvida
» Dúvida Estequiometria - Exercício ITA
» Dúvida - Exercícios de Estequiometria
» Dúvida de enunciado de estéquiometria.
» Estequiometria - Dúvida
» Dúvida Estequiometria - Exercício ITA
» Dúvida - Exercícios de Estequiometria
» Dúvida de enunciado de estéquiometria.
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













