Transformação Química
4 participantes
Página 1 de 1
 Transformação Química
Transformação Química
(Fuvest-SP) Nitrato de bário pode ser preparado, em meio aquoso, através das transformações químicas abaixo:
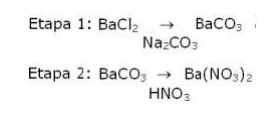
Nas etapas 1 e 2, ocorrem, respectivamente:
a) precipitação de carbonato de bário e desprendimento de dióxido de carbono.
b) precipitação de carbonato de bário e desprendimento de hidrogênio.
c) desprendimento de cloro e desprendimento de dióxido de carbono.
d) desprendimento de dióxido de carbono e precipitação de nitrato de bário.
e) desprendimento de cloro e neutralização do carbonato de bário.
GAB: A
Como faço essa questão?
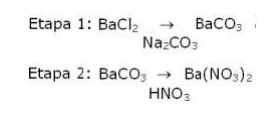
Nas etapas 1 e 2, ocorrem, respectivamente:
a) precipitação de carbonato de bário e desprendimento de dióxido de carbono.
b) precipitação de carbonato de bário e desprendimento de hidrogênio.
c) desprendimento de cloro e desprendimento de dióxido de carbono.
d) desprendimento de dióxido de carbono e precipitação de nitrato de bário.
e) desprendimento de cloro e neutralização do carbonato de bário.
GAB: A
Como faço essa questão?

Augusto H.- Mestre Jedi

- Mensagens : 509
Data de inscrição : 22/03/2017
Idade : 25
Localização : Porto Alegre
 Re: Transformação Química
Re: Transformação Química
Etapa 1: BaCl2 + Na2CO3 -> BaCO3 + 2NaCl
Assumindo previamente que está ocorrendo em meio aquoso, sabe-se que carbonatos são insolúveis. Portanto, o carbonato de bário precipitará.
Etapa 2: BaCO3 + 2HNO3 -> Ba(NO3)2 + H2CO3
H2CO3 é instável, se decompõe e forma CO2 e água.
Espero ter ajudado, caso contrário, qual a dúvida mais explicitamente?
Assumindo previamente que está ocorrendo em meio aquoso, sabe-se que carbonatos são insolúveis. Portanto, o carbonato de bário precipitará.
Etapa 2: BaCO3 + 2HNO3 -> Ba(NO3)2 + H2CO3
H2CO3 é instável, se decompõe e forma CO2 e água.
Espero ter ajudado, caso contrário, qual a dúvida mais explicitamente?

MalcolnMed- Mestre Jedi

- Mensagens : 705
Data de inscrição : 03/04/2017
Idade : 26
Localização : São Paulo
 Re: Transformação Química
Re: Transformação Química
Certo, estava com dificuldade na etapa 2, mas compreendi agora.
Obrigado MalcolnMed!
Obrigado MalcolnMed!

Augusto H.- Mestre Jedi

- Mensagens : 509
Data de inscrição : 22/03/2017
Idade : 25
Localização : Porto Alegre
 Re: Transformação Química
Re: Transformação Química
Perdao por ressuscitar o post, mas teria alguma forma de saber que H2CO3 é instavel ou é algo obtido experimentalmente?
aguahomem- Iniciante
- Mensagens : 5
Data de inscrição : 26/10/2018
Idade : 20
Localização : Belo Horizonte, Minas Gerais - Brasil
 Re: Transformação Química
Re: Transformação Química
Oi, não acho que tem como você deduzir na hora da questão, mas a instabilidade do H2CO3 é bem conhecida, mas na realidade H2CO3 é um composto estável, o que ocorre é que H2O e CO2 são muito estáveis, e a espontaneidade da reação no sentido de formar H2O e CO2 é maior pois é uma reação exotérmica.

Leo Consoli- Fera

- Mensagens : 383
Data de inscrição : 03/08/2017
Idade : 23
Localização : Salvador, Bahia, Brasil
 Tópicos semelhantes
Tópicos semelhantes» Transformação química
» transformação química
» Transformação química ou física
» Estudar Físico-química ou química orgânica
» Reação Química e Equação Química
» transformação química
» Transformação química ou física
» Estudar Físico-química ou química orgânica
» Reação Química e Equação Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos












