Gás Ideal
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Gás Ideal
Gás Ideal
(UEFS-2011)Referindo-se ao estado final de um gás ideal que foi expandido adiabaticamente, é correto afirmar:
A) A temperatura do gás aumenta.
B) A temperatura do gás diminui.
C) A energia interna do gás aumenta.
D) A energia interna do gás se mantém constante.
E) A variação de energia interna do gás é igual à quantidade de calor trocado com o meio exterior.
GAB: B
OBS: Para mim, deu letra D, pois como o gás está expandindo o V>0 e como o processo é adiabático a T=0, consequentemente a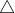 U=0.
U=0.
A) A temperatura do gás aumenta.
B) A temperatura do gás diminui.
C) A energia interna do gás aumenta.
D) A energia interna do gás se mantém constante.
E) A variação de energia interna do gás é igual à quantidade de calor trocado com o meio exterior.
GAB: B
OBS: Para mim, deu letra D, pois como o gás está expandindo o V>0 e como o processo é adiabático a T=0, consequentemente a
Última edição por Anna Georgia em Qui 29 Jul 2021, 19:08, editado 1 vez(es)

Anna Georgia- Padawan

- Mensagens : 50
Data de inscrição : 11/07/2019
Idade : 25
Localização : São Gonçalo, RJ
 Re: Gás Ideal
Re: Gás Ideal
Olá Anna!
Em transformações adiabáticas, não se tem troca de calor com os meios, não que a temperatura do sistema seja nula. A letra B é coerente, em uma expansão adiabática as moléculas se distanciam, logo a pressão do gás e a temperatura também diminuem.
''OBS: Para mim, deu letra D, pois como o gás está expandindo o V>0 e como o processo é adiabático a T=0, consequentemente a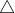 U=0.''
U=0.''
I - Todo volume é positivo, sua relação está correta, mas acho que o que você quis dizer é que o Volume final > Volume inicial.
II - Como a transformação ocorre de maneira quase que instantânea, o calor não é trocado com o meio, logo, Q = 0. Usando o princípio da primeira lei da termodinâmica: Q = W + ∆U => ∆U = -W, toda a energia interna é convertida em trabalho, o sinal negativo condiz pois como não há uma fonte de calor, para o gás se expandir o gás precisa realizar trabalho no meio.
Espero ter ajudado.
Em transformações adiabáticas, não se tem troca de calor com os meios, não que a temperatura do sistema seja nula. A letra B é coerente, em uma expansão adiabática as moléculas se distanciam, logo a pressão do gás e a temperatura também diminuem.
''OBS: Para mim, deu letra D, pois como o gás está expandindo o V>0 e como o processo é adiabático a T=0, consequentemente a
I - Todo volume é positivo, sua relação está correta, mas acho que o que você quis dizer é que o Volume final > Volume inicial.
II - Como a transformação ocorre de maneira quase que instantânea, o calor não é trocado com o meio, logo, Q = 0. Usando o princípio da primeira lei da termodinâmica: Q = W + ∆U => ∆U = -W, toda a energia interna é convertida em trabalho, o sinal negativo condiz pois como não há uma fonte de calor, para o gás se expandir o gás precisa realizar trabalho no meio.
Espero ter ajudado.

qedpetrich- Monitor

- Mensagens : 2497
Data de inscrição : 05/07/2021
Idade : 24
Localização : Erechim - RS / Passo Fundo - RS
murillous gosta desta mensagem
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














