Estrutura do ácido fosfórico ?
+3
BatataDoFuturo
Thálisson C
OldFears
7 participantes
Página 2 de 2
Página 2 de 2 •  1, 2
1, 2
 Estrutura do ácido fosfórico ?
Estrutura do ácido fosfórico ?
Relembrando a primeira mensagem :
Estava estudando ácidos em um livro, aí fiquei com uma dúvida no ácido fosfórico, veja :
O ácido fosfórico tem forma química H3PO4 . (3 hidrogênios , 1 fósforo e 4 oxigênios).
a forma estrutural do ácido fosfórico :
OH -.
OH --- P--> O
OH -'
No ácido fosforoso , a forma é H3PO3.
a forma estrutural do ácido fosforoso :
OH -.
OH --- P ---> O
H -'
eu queria saber , por qual motivo a forma estrutural do ácido fosforoso não pode ser assim :
OH -.
OH ---P
OH -'
dessa forma, haveria as 3 ligações necessárias pro fósforo, e os 3 oxigênios e os 3 hidrogênios. Por qual motivo não pode ser assim?
e outra, do ácido nítrico (HNO3)
por qual motivo a fórmula química não poderia ser H3NO3? ficando a forma estrutural assim :
OH -.
OH -- N
OH -'
Fiquei com essa dúvida, pois depois de um tempo se eu não lembrar a formula do ácido, eu poder deduzir através da quantidade de elétrons na camada de valência.
Desde já agradeço, valeu !!
Estava estudando ácidos em um livro, aí fiquei com uma dúvida no ácido fosfórico, veja :
O ácido fosfórico tem forma química H3PO4 . (3 hidrogênios , 1 fósforo e 4 oxigênios).
a forma estrutural do ácido fosfórico :
OH -.
OH --- P--> O
OH -'
No ácido fosforoso , a forma é H3PO3.
a forma estrutural do ácido fosforoso :
OH -.
OH --- P ---> O
H -'
eu queria saber , por qual motivo a forma estrutural do ácido fosforoso não pode ser assim :
OH -.
OH ---P
OH -'
dessa forma, haveria as 3 ligações necessárias pro fósforo, e os 3 oxigênios e os 3 hidrogênios. Por qual motivo não pode ser assim?
e outra, do ácido nítrico (HNO3)
por qual motivo a fórmula química não poderia ser H3NO3? ficando a forma estrutural assim :
OH -.
OH -- N
OH -'
Fiquei com essa dúvida, pois depois de um tempo se eu não lembrar a formula do ácido, eu poder deduzir através da quantidade de elétrons na camada de valência.
Desde já agradeço, valeu !!
OldFears- Jedi

- Mensagens : 229
Data de inscrição : 02/01/2013
Idade : 26
Localização : Botucatu-Sp , Brasil
 Re: Estrutura do ácido fosfórico ?
Re: Estrutura do ácido fosfórico ?
Ligações dativas não existem. São um artifício para induzir explicações de nível médio.
Marcelo F- Jedi

- Mensagens : 368
Data de inscrição : 29/05/2015
Idade : 31
Localização : Rio de janeiro
 Re: Estrutura do ácido fosfórico ?
Re: Estrutura do ácido fosfórico ?
Sim sim, mas então o modelo que seguimos só serve para explicar as ligações e não pode prevê-las?
BatataDoFuturo- Recebeu o sabre de luz

- Mensagens : 173
Data de inscrição : 13/08/2015
Idade : 34
Localização : Bauru-SP
 Re: Estrutura do ácido fosfórico ?
Re: Estrutura do ácido fosfórico ?
Com os conhecimentos de nível médio, é possível chegar a uma conclusão sem usar a teoria do orbital molecular, aprendida em nível superior:
Elementos do primeiro e segundo nunca poderão expandir seu octeto pois as suas camadas de valência, suportam no máximo, os oito supostos elétrons necessários a estabilidade:
1º período - > Nível 1 -> suporta no máximo 2 elétrons
2º período - > Nível 2 -> suporta no máximo 8 elétrons
Agora se observarmos elementos do 3 período, onde o nível máximo é 3:
3º período -> nível 3 -> suporta no máximo 18 elétrons
Isso porque elementos do terceiro período em diante podem ter o orbital d em suas configurações eletrônicas, e com isso podem ter mais de oito elétrons na última camada.
Percebam que os elementos do primeiro e segundo período só não expandem seu octeto porque necessariamente eles não podem fazê-lo.
A regra do octeto se mostra então, muito limitada. A teoria das cargas formais ajudam a prever estruturas e devemos utilizá-la.
As cargas formais de cada elemento em uma molécula devem ser mínimas para estabilidade da mesma, e em cada elemento pode ser calculada como:
C = (Nº de elétrons de valência) - (Nº de elétrons livres) - (Nº de elétrons ligantes)/2
A grande discussão é a respeito do ácido fosforoso, cuja estrutura de lewis pode ser montada assim:
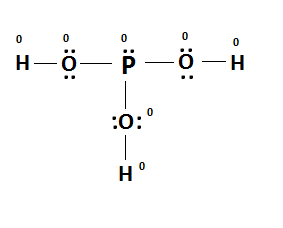
Essa é uma configuração onde, todas as cargas formais são zero e o fosforo obedece ao octeto.
Entretanto, o fósforo é um elemento do terceiro período, ele não necessariamente se estabilizará com oitos elétrons em sua camada de valência, então, por que deveria ser esta a estrutura correta, se a teoria do octeto é apenas uma tendência de elementos que suportam esses oito elétrons na última camada ?
A fórmula estrutural real do ácido fosforoso é a seguinte:
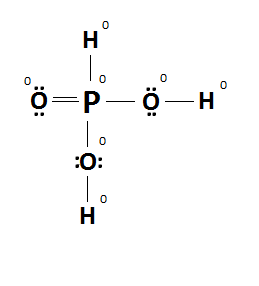
As cargas formais continuam dando o menor valor possível para cada elemento, com a diferença que o fósforo se estabiliza com dez elétrons na última camada.
Obedecer ou não ao octeto ? Como o fósforo pode ter mais que oito elétrons na última camada, não necessariamente ele obedece, se trata novamente de uma teoria muito limitada (minha opinião).
No ensino médio "troca-se" no lugar daquela ligação dupla entre o fósforo e o oxigênio, por uma ligação covalente dativa ou coordenada, de modo que o fósforo permaneça com oito elétrons na última camada, essa é apenas uma estratégia didática, para os alunos pensarem que a regra do octeto é "indiscutível" e que, após chegar até aqui, isso ficou claro que não é verdade.
Elementos do primeiro e segundo nunca poderão expandir seu octeto pois as suas camadas de valência, suportam no máximo, os oito supostos elétrons necessários a estabilidade:
1º período - > Nível 1 -> suporta no máximo 2 elétrons
2º período - > Nível 2 -> suporta no máximo 8 elétrons
Agora se observarmos elementos do 3 período, onde o nível máximo é 3:
3º período -> nível 3 -> suporta no máximo 18 elétrons
Isso porque elementos do terceiro período em diante podem ter o orbital d em suas configurações eletrônicas, e com isso podem ter mais de oito elétrons na última camada.
Percebam que os elementos do primeiro e segundo período só não expandem seu octeto porque necessariamente eles não podem fazê-lo.
A regra do octeto se mostra então, muito limitada. A teoria das cargas formais ajudam a prever estruturas e devemos utilizá-la.
As cargas formais de cada elemento em uma molécula devem ser mínimas para estabilidade da mesma, e em cada elemento pode ser calculada como:
C = (Nº de elétrons de valência) - (Nº de elétrons livres) - (Nº de elétrons ligantes)/2
A grande discussão é a respeito do ácido fosforoso, cuja estrutura de lewis pode ser montada assim:

Essa é uma configuração onde, todas as cargas formais são zero e o fosforo obedece ao octeto.
Entretanto, o fósforo é um elemento do terceiro período, ele não necessariamente se estabilizará com oitos elétrons em sua camada de valência, então, por que deveria ser esta a estrutura correta, se a teoria do octeto é apenas uma tendência de elementos que suportam esses oito elétrons na última camada ?
A fórmula estrutural real do ácido fosforoso é a seguinte:

As cargas formais continuam dando o menor valor possível para cada elemento, com a diferença que o fósforo se estabiliza com dez elétrons na última camada.
Obedecer ou não ao octeto ? Como o fósforo pode ter mais que oito elétrons na última camada, não necessariamente ele obedece, se trata novamente de uma teoria muito limitada (minha opinião).
No ensino médio "troca-se" no lugar daquela ligação dupla entre o fósforo e o oxigênio, por uma ligação covalente dativa ou coordenada, de modo que o fósforo permaneça com oito elétrons na última camada, essa é apenas uma estratégia didática, para os alunos pensarem que a regra do octeto é "indiscutível" e que, após chegar até aqui, isso ficou claro que não é verdade.
____________________________________________
Thálisson.

Thálisson C- Monitor

- Mensagens : 3020
Data de inscrição : 19/02/2014
Idade : 27
Localização : Gurupi -TO
 Re: Estrutura do ácido fosfórico ?
Re: Estrutura do ácido fosfórico ?
Teoria limitada, mas necessária para uma mais fácil compreensão por parte dos alunos de nível médio.
 Re: Estrutura do ácido fosfórico ?
Re: Estrutura do ácido fosfórico ?
@Thálisson C
Algum livro que você recomenda que possa me ajudar a prever essas estruturas?
Obs: Fiquei com uma dúvida, então as cargas formais só podem ser utilizadas para definir a melhor estrutura para átomos que obedeçam à regra do octeto?
Algum livro que você recomenda que possa me ajudar a prever essas estruturas?
Obs: Fiquei com uma dúvida, então as cargas formais só podem ser utilizadas para definir a melhor estrutura para átomos que obedeçam à regra do octeto?
BatataDoFuturo- Recebeu o sabre de luz

- Mensagens : 173
Data de inscrição : 13/08/2015
Idade : 34
Localização : Bauru-SP
 Re: Estrutura do ácido fosfórico ?
Re: Estrutura do ácido fosfórico ?
Não posso dizer quanto aos livros, desculpe.
Mas o melhor é tentar fazer as estruturas de várias moléculas, observando as cargas formais e a expansão (ou contração no octeto) e depois ver as estruturas reais e comparar.
As cargas formais podem ser observadas independente da estrutura seguir ou não a regra do octeto.
Mas o melhor é tentar fazer as estruturas de várias moléculas, observando as cargas formais e a expansão (ou contração no octeto) e depois ver as estruturas reais e comparar.
As cargas formais podem ser observadas independente da estrutura seguir ou não a regra do octeto.
____________________________________________
Thálisson.

Thálisson C- Monitor

- Mensagens : 3020
Data de inscrição : 19/02/2014
Idade : 27
Localização : Gurupi -TO
 Re: Estrutura do ácido fosfórico ?
Re: Estrutura do ácido fosfórico ?
Thálisson C, só uma duvida: Por que a segunda é a correta? Quero dizer, eu entendi que poderia ser as duas, mas por que é a segunda e não a primeira? Por que a segunda forma de representação prevalece sobre a primeira? :scratch:

EstudanteCiencias- Jedi

- Mensagens : 358
Data de inscrição : 17/07/2016
Idade : 25
Localização : Salvador - Bahia
Página 2 de 2 •  1, 2
1, 2
 Tópicos semelhantes
Tópicos semelhantes» Ácido Fosfórico
» Acido Fosforico
» Hidróxido de calcio + ácido fosfórico?
» Estrutura
» Sobre fórmula do ácido fosfórico
» Acido Fosforico
» Hidróxido de calcio + ácido fosfórico?
» Estrutura
» Sobre fórmula do ácido fosfórico
Página 2 de 2
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














