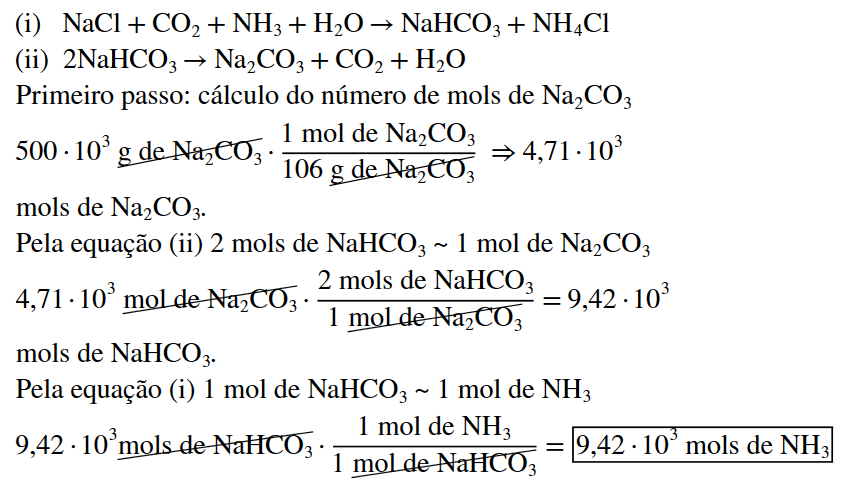Calculo Estequiométrico
2 participantes
Página 1 de 1
 Calculo Estequiométrico
Calculo Estequiométrico
O carbonato de sódio (Na2CO3), importante matéria-prima na fabricação de vidros, pode ser produzido a partir da reação do cloreto de sódio, amônia e gás carbônico, processo químico conhecido como processo Solvay. São apresentadas duas etapas deste processo.
Etapa I: NaCl + CO2 + NH3 + H2O → NaHCO3 + NH4Cl
Etapa II: 2NaHCO3 → Na2CO3 + CO2 + H2O
Considerando que o rendimento da reação é 100%, calcule o volume de amônia (NH3) necessário para produzir 500 kg carbonato de sódio.
Não possuo gabarito.
Etapa I: NaCl + CO2 + NH3 + H2O → NaHCO3 + NH4Cl
Etapa II: 2NaHCO3 → Na2CO3 + CO2 + H2O
Considerando que o rendimento da reação é 100%, calcule o volume de amônia (NH3) necessário para produzir 500 kg carbonato de sódio.
Não possuo gabarito.

TrailRunner- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 09/04/2016
Idade : 30
Localização : Belo Horizonte
 Re: Calculo Estequiométrico
Re: Calculo Estequiométrico
____________________________________________
El Álgebra no es más que Geometría y la Geometría no es más que Álgebra abstracta
Sophie Germain
Sophie Germain
Emanuel Dias- Monitor

- Mensagens : 1703
Data de inscrição : 15/12/2018
Idade : 22
Localização : São Paulo
 Re: Calculo Estequiométrico
Re: Calculo Estequiométrico
Emanuel, eu calculei dessa forma:

O que eu fiz foi começar caculando da equação 2 para equação 1.
No caso eu achei a quantidade de 2NaHCO3 para 500KG de Na2CO3.
Como na equação 1 temoso 1 mol apenas de NaHCO3, eu dividi o valor encontrado por 2.
Para encontrar o volume, eu usei a seguinte relação:
1 mol = 22,4L.
Como tinhamos 1 mol de NH3, montei a regra de 3 e achei o valor. Está errado?

O que eu fiz foi começar caculando da equação 2 para equação 1.
No caso eu achei a quantidade de 2NaHCO3 para 500KG de Na2CO3.
Como na equação 1 temoso 1 mol apenas de NaHCO3, eu dividi o valor encontrado por 2.
Para encontrar o volume, eu usei a seguinte relação:
1 mol = 22,4L.
Como tinhamos 1 mol de NH3, montei a regra de 3 e achei o valor. Está errado?

TrailRunner- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 09/04/2016
Idade : 30
Localização : Belo Horizonte
 Re: Calculo Estequiométrico
Re: Calculo Estequiométrico
A imagem ficou muito pequena, algumas partes não consigo ler.
Você foi por um caminho diferente, mas equivalente, acredito eu.
A questão é, essa relação 22 L/mol ocorre apenas nas CNTP, então teria que ter dito isso no enunciado: pV=nRt
V=nRt/P
Se n=1 V=Rt/P se substituir os valores da CNTP o resultado é 22,4 L.
Você foi por um caminho diferente, mas equivalente, acredito eu.
A questão é, essa relação 22 L/mol ocorre apenas nas CNTP, então teria que ter dito isso no enunciado: pV=nRt
V=nRt/P
Se n=1 V=Rt/P se substituir os valores da CNTP o resultado é 22,4 L.
____________________________________________
El Álgebra no es más que Geometría y la Geometría no es más que Álgebra abstracta
Sophie Germain
Sophie Germain
Emanuel Dias- Monitor

- Mensagens : 1703
Data de inscrição : 15/12/2018
Idade : 22
Localização : São Paulo
 Re: Calculo Estequiométrico
Re: Calculo Estequiométrico
____________________________________________
El Álgebra no es más que Geometría y la Geometría no es más que Álgebra abstracta
Sophie Germain
Sophie Germain
Emanuel Dias- Monitor

- Mensagens : 1703
Data de inscrição : 15/12/2018
Idade : 22
Localização : São Paulo
 Re: Calculo Estequiométrico
Re: Calculo Estequiométrico
Obrigado!!

TrailRunner- Recebeu o sabre de luz

- Mensagens : 102
Data de inscrição : 09/04/2016
Idade : 30
Localização : Belo Horizonte
 Tópicos semelhantes
Tópicos semelhantes» Calculo estequiométrico
» Cálculo estequiométrico
» cálculo estequiométrico
» Cálculo estequiométrico
» Cálculo Estequiométrico(IME)
» Cálculo estequiométrico
» cálculo estequiométrico
» Cálculo estequiométrico
» Cálculo Estequiométrico(IME)
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos