DESAFIO - Termodinânica
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 DESAFIO - Termodinânica
DESAFIO - Termodinânica
Um gás ideal inicialmente a temperatura \theta 1 sofre uma transformação adiabática reversível, sabendo que a temperatura final é \theta 2, dados os calores específico dos gases ideal cp e cv, para transformações a pressão e volume constante respectivamente, explique:
a) Por que o trabalho é dado por W=Qp-Qv (onde Qp, Qv é a quantidade de calor recebida pelo gás, quando este sofre transformações a pressão e volume constantes respectivamente, nas condições citadas)
b) Calcule o trabalho realizado pelo gás na transformação citada.
c) Para uma transformação isométrica temos \Delta Uv=Qv (trabalho nulo), e para uma transformação com a mesma variação de temperatura \Delta U=\Delta Uv, onde \Delta U é a variação de energia interna do gás a pressão e volume variáveis, porque então não podemos no item A expressar \Delta U=-W=\Delta Uv=Qv já que Qv\neq Qp-Qv
a) Por que o trabalho é dado por W=Qp-Qv (onde Qp, Qv é a quantidade de calor recebida pelo gás, quando este sofre transformações a pressão e volume constantes respectivamente, nas condições citadas)
b) Calcule o trabalho realizado pelo gás na transformação citada.
c) Para uma transformação isométrica temos \Delta Uv=Qv (trabalho nulo), e para uma transformação com a mesma variação de temperatura \Delta U=\Delta Uv, onde \Delta U é a variação de energia interna do gás a pressão e volume variáveis, porque então não podemos no item A expressar \Delta U=-W=\Delta Uv=Qv já que Qv\neq Qp-Qv
 Re: DESAFIO - Termodinânica
Re: DESAFIO - Termodinânica
a) Na transformação isobárica, o aquecimento deve sempre vir acompanhado de um trabalho, já que é necessário um aumento de volume para que a pressão permaneça constante, isto é, para que as colisões das partículas de gás nas paredes do recipiente permaneçam num número constante. Logo, pela primeira lei da termodinâmica:
A volume constante, o sistema não realizará trabalho, o que implica:
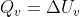
E para pressão constante:
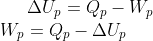
Não obstante, se o aquecimento é feito a volume e pressão constantes, a variação de energia interna na transformação isométrica é a mesma da transformação isobárica:
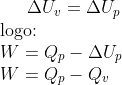
b)
\underbrace{(Cp-Cv)}_{R,\,\text{relacao&space;de&space;Mayer}}\\W=n.R(\theta&space;_{2}-\theta&space;_{1}))
Como era esperado.
Não fiz a c pois eu realmente não entendi o que digitou.
A volume constante, o sistema não realizará trabalho, o que implica:
E para pressão constante:
Não obstante, se o aquecimento é feito a volume e pressão constantes, a variação de energia interna na transformação isométrica é a mesma da transformação isobárica:
b)
Como era esperado.
Não fiz a c pois eu realmente não entendi o que digitou.
Última edição por Willian Honorio em Sáb 27 maio 2017, 19:13, editado 1 vez(es)

Willian Honorio- Matador

- Mensagens : 1271
Data de inscrição : 27/04/2016
Idade : 27
Localização : São Paulo
 Re: DESAFIO - Termodinânica
Re: DESAFIO - Termodinânica
Deu pra entender um pouco mais porque você considerou que o trabalho é constante? essa parte não entendi, no enunciado ele diz apenas que a transformação é adiabática e reversível que transformação seria essa? ficaria mais claro se explicasse o raciocínio. Em uma transformação adiabática sei que DeltaU=-W mas porque Wp(trabalho a pressão constante)?
Não sei se entendeu minha duvida
Obrigado desde já...
E porque será que o latex não está funcionando pra mim? algum moderador ai?
Não sei se entendeu minha duvida
Obrigado desde já...
E porque será que o latex não está funcionando pra mim? algum moderador ai?
 Re: DESAFIO - Termodinânica
Re: DESAFIO - Termodinânica
Isso significado que o gás não cederá calor para o meio externo, sua entropia permanecerá constante, e que ele pode voltar à suas condições iniciais sem a interferência de um agente externo realizando trabalho (transformação reversível). Nas alternativas, ele refere-se a uma transformação isométrica precedida de uma adiabática. O trabalho pedido é o trabalho da transformação citada. O trabalho não é constante, a pressão constante é uma coisa e a volume é outra, a única variável constante é a energia interna do sistema na transformações.

Willian Honorio- Matador

- Mensagens : 1271
Data de inscrição : 27/04/2016
Idade : 27
Localização : São Paulo
 Re: DESAFIO - Termodinânica
Re: DESAFIO - Termodinânica
Eu queria dizer trabalho a pressão constante, escrevi errado haha.
A minha dúvida era, aqui:
Para uma mesma variação de temperatura não importa qual o processo isobárico ou isométrico a variação de energia interna vai ser a mesma ok.
Mas através do que você fez na manipulação das fórmulas e chegou ao trabalho W=Qp-Qv
Ele vem de Wp=Qp-DUp certo?
Esse trabalho seria se a transformação fosse a pressão constante para a mesma variação de temperatura que a transformação ADIABÁTICA foi feita.
Logo como pode-se afirmar que os trabalhos dos dois tipos de transformação são iguais?
Imaginando um gráfico com dois isotermas, e 2 transformação de um isoterma para o outro, 1 transformação isobárica e outra adiabática a área será diferente, não?
Desculpe a ignorância, mas termodinâmica ta sendo uma matéria difícil pra mim haha.
A minha dúvida era, aqui:
Para uma mesma variação de temperatura não importa qual o processo isobárico ou isométrico a variação de energia interna vai ser a mesma ok.
Mas através do que você fez na manipulação das fórmulas e chegou ao trabalho W=Qp-Qv
Ele vem de Wp=Qp-DUp certo?
Esse trabalho seria se a transformação fosse a pressão constante para a mesma variação de temperatura que a transformação ADIABÁTICA foi feita.
Logo como pode-se afirmar que os trabalhos dos dois tipos de transformação são iguais?
Imaginando um gráfico com dois isotermas, e 2 transformação de um isoterma para o outro, 1 transformação isobárica e outra adiabática a área será diferente, não?
Desculpe a ignorância, mas termodinâmica ta sendo uma matéria difícil pra mim haha.
 Re: DESAFIO - Termodinânica
Re: DESAFIO - Termodinânica
Você está se perdendo apenas no enunciado da questão. O fato dele dizer que a transformação é adiabática diz apenas que o sistema não desperdiçará energia para o meio externo, parte da energia absorvida será para aumentar a energia interna das moléculas de gás e parte absorvida para realizar trabalho sobre um êmbolo. Em seguida, o trabalho que ele nos pede é o de uma transformação isobárica seguida por uma isocórica.
Geralmente as dificuldades em termodinâmica surgem devido a um estudo superficial dos gases, por exemplo, você não entenderá eletrodinâmica sem entender eletrostática, nem MRUV sem entender MRU, o mesmo vale para termodinâmica e gases. Só faço uma observação: não posso ensinar teoria. Não sou professor, tampouco possuo essa qualificação, se eu te falar uma besteira você pode futuramente errar uma questão num vestibular, por exemplo. Nessa equação Wp=Qp-Qv, você encontrará num livro a equação melhor demonstrada (mesmo a minha estando correta), e assuntos que irão superpor em quase 100% o que abordei acima e de maneira didática e mascada. Digo isso, num tom amigável, pois meu intuito é apenas lhe ajudar a resolver o problema com um pouco de teoria que penso que sei.
Geralmente as dificuldades em termodinâmica surgem devido a um estudo superficial dos gases, por exemplo, você não entenderá eletrodinâmica sem entender eletrostática, nem MRUV sem entender MRU, o mesmo vale para termodinâmica e gases. Só faço uma observação: não posso ensinar teoria. Não sou professor, tampouco possuo essa qualificação, se eu te falar uma besteira você pode futuramente errar uma questão num vestibular, por exemplo. Nessa equação Wp=Qp-Qv, você encontrará num livro a equação melhor demonstrada (mesmo a minha estando correta), e assuntos que irão superpor em quase 100% o que abordei acima e de maneira didática e mascada. Digo isso, num tom amigável, pois meu intuito é apenas lhe ajudar a resolver o problema com um pouco de teoria que penso que sei.

Willian Honorio- Matador

- Mensagens : 1271
Data de inscrição : 27/04/2016
Idade : 27
Localização : São Paulo
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














