(FUVEST) Equilíbrio Químico
3 participantes
Página 1 de 1
 (FUVEST) Equilíbrio Químico
(FUVEST) Equilíbrio Químico
A reação de persulfato com iodeto
S2O8 (2-) + 2I (-) --------> 2 SO4 (2-) + I2
pode ser acompanhada pelo aparecimento da cor do iodo. Se no início da reação persulfato e
iodeto estiverem em proporção estequiométrica (1:2), as concentrações de persulfato e de
iodeto, em função do tempo de reação, serão representadas pelo gráfico:

--
Gabarito:B
Fiquei em dúvida entre A, B e D. (Até onde a reta dos reagentes vai? Como descubro isso?)
S2O8 (2-) + 2I (-) --------> 2 SO4 (2-) + I2
pode ser acompanhada pelo aparecimento da cor do iodo. Se no início da reação persulfato e
iodeto estiverem em proporção estequiométrica (1:2), as concentrações de persulfato e de
iodeto, em função do tempo de reação, serão representadas pelo gráfico:

--
Gabarito:B
Fiquei em dúvida entre A, B e D. (Até onde a reta dos reagentes vai? Como descubro isso?)

MuriloTri- Mestre Jedi

- Mensagens : 636
Data de inscrição : 13/03/2012
Idade : 28
Localização : Campinas
 Re: (FUVEST) Equilíbrio Químico
Re: (FUVEST) Equilíbrio Químico
Os reagentes foram colocados na solução em proporção de 1:2 (item C e E descartados)
Por cinética química, sabe-se que a velocidade de consumo dos reagentes é proporcional ao coeficiente na reação. Logo: (Sendo Vc, velocidade de consumo)
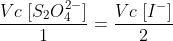
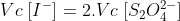 --> Já se descarta o item A
--> Já se descarta o item A
Ainda pela proporção estequiométrica, e notando que, em todos itens, ao final da reação coexistem os reagentes (há um equilíbrio químico) pode-se fazer uma tabela:
------------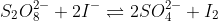
Início:---- 5 M ------ 10 M----- 0 -------- 0
Variação:- -x ------ -2x ------ +2x ----- +x
Final: --- (5-x) M--(10-2x) M-- 2x ------ x
O número de mols consumidos de S2O8{2-} foi a metade do consumido por I{-}.
Avaliando os gráficos quadriculados:
Item B --> Foram consumidos 8 quadrados de I{-} e 4 quadrados de S2O8{2-} --> Item Correto.
Por cinética química, sabe-se que a velocidade de consumo dos reagentes é proporcional ao coeficiente na reação. Logo: (Sendo Vc, velocidade de consumo)
Ainda pela proporção estequiométrica, e notando que, em todos itens, ao final da reação coexistem os reagentes (há um equilíbrio químico) pode-se fazer uma tabela:
------------
Início:---- 5 M ------ 10 M----- 0 -------- 0
Variação:- -x ------ -2x ------ +2x ----- +x
Final: --- (5-x) M--(10-2x) M-- 2x ------ x
O número de mols consumidos de S2O8{2-} foi a metade do consumido por I{-}.
Avaliando os gráficos quadriculados:
Item B --> Foram consumidos 8 quadrados de I{-} e 4 quadrados de S2O8{2-} --> Item Correto.

schow- Jedi

- Mensagens : 446
Data de inscrição : 03/01/2013
Idade : 28
Localização : Fortaleza-CE
 Re: (FUVEST) Equilíbrio Químico
Re: (FUVEST) Equilíbrio Químico
Perfeito, Obrigado!

MuriloTri- Mestre Jedi

- Mensagens : 636
Data de inscrição : 13/03/2012
Idade : 28
Localização : Campinas
 Re: (FUVEST) Equilíbrio Químico
Re: (FUVEST) Equilíbrio Químico
Galera, poderiamos descartar a letra D assim: No grafico D, há uma variação de 8mol.L-¹/s e 3mol.L-¹/s entre os instantes t=0 e t=1?

EstudanteCiencias- Jedi

- Mensagens : 358
Data de inscrição : 17/07/2016
Idade : 24
Localização : Salvador - Bahia
 Tópicos semelhantes
Tópicos semelhantes» Equilíbrio químico - FUVEST
» Equilíbrio Químico - Fuvest
» FUVEST-Equilíbrio Químico
» (fuvest) equilíbrio químico e constante
» (fuvest) equilibrio quimico
» Equilíbrio Químico - Fuvest
» FUVEST-Equilíbrio Químico
» (fuvest) equilíbrio químico e constante
» (fuvest) equilibrio quimico
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













