Equilíbrio Químico e Pressão
3 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Equilíbrio Químico e Pressão
Equilíbrio Químico e Pressão
(UPE)A decomposição térmica do bicarbonato de sódio apresenta importância industrial, por ser a última etapa do processo Solvay de fabricação de soda. Na reprodução desse processo, em um laboratório de pesquisa de uma universidade, uma amostra de 100 g de bicarbonato de sódio foi colocada em um recipiente de 2,46 litros, totalmente vedado e aquecido até 87ºC, estabelecendo o equilíbrio representado a seguir:
2 NaHCO3(s) Na2CO3(s) + H2O(g) + CO2(g)
Na2CO3(s) + H2O(g) + CO2(g)
Nessas condições, a constante de equilíbrio é igual a 36.
Dados: 1 bar ≈ 1 atm; R = 0,082 atm.L.mol-1.K-1; Massas atômicas: H = 1 u; C = 12 u; O = 16 u; Na = 23 u
Quando o equilíbrio desse sistema foi estabelecido, a pressão total e a massa de carbonato de sódio produzida tinham valores, respectivamente, de
R: 12 atm e 53g
Alguém poderia,por favor,me ajudar?
2 NaHCO3(s)
Nessas condições, a constante de equilíbrio é igual a 36.
Dados: 1 bar ≈ 1 atm; R = 0,082 atm.L.mol-1.K-1; Massas atômicas: H = 1 u; C = 12 u; O = 16 u; Na = 23 u
Quando o equilíbrio desse sistema foi estabelecido, a pressão total e a massa de carbonato de sódio produzida tinham valores, respectivamente, de
R: 12 atm e 53g
Alguém poderia,por favor,me ajudar?
Última edição por MiLory em Dom 24 Out 2021, 15:22, editado 1 vez(es)

MiLory- Iniciante
- Mensagens : 9
Data de inscrição : 20/07/2020
Idade : 21

jopagliarin- Jedi

- Mensagens : 399
Data de inscrição : 13/10/2019
Idade : 22
Localização : Curitiba/PR \\ Joaçaba/SC
 Re: Equilíbrio Químico e Pressão
Re: Equilíbrio Químico e Pressão
Olá, tudo certo?
Temos o seguinte equilíbrio.

In: ~ ~ ∅ ∅
R: ~ ~ +x +x
Eq: ~ ~ x x
Assim, pressupondo que essa constante de equilíbrio seja em relação às pressões:
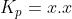
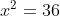
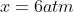
Assim, a pressão total final do sistema é:

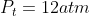
Pela equação de Clapeyron:

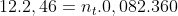
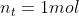
Agora, observe que, pela proporção estequiométrica, formam-se iguais quantidades de matéria de CO2 e H2O. Desse modo, temos:
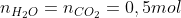
De tal maneira, também, pela proporção estequiométrica dos produtos- 1:1:1- temos:
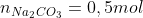
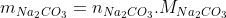
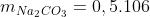
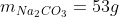
Espero ter ajudado! Grande Abraço!
Temos o seguinte equilíbrio.
In: ~ ~ ∅ ∅
R: ~ ~ +x +x
Eq: ~ ~ x x
Assim, pressupondo que essa constante de equilíbrio seja em relação às pressões:
Assim, a pressão total final do sistema é:
Pela equação de Clapeyron:
Agora, observe que, pela proporção estequiométrica, formam-se iguais quantidades de matéria de CO2 e H2O. Desse modo, temos:
De tal maneira, também, pela proporção estequiométrica dos produtos- 1:1:1- temos:
Espero ter ajudado! Grande Abraço!

FocoNoIMEITA- Jedi

- Mensagens : 270
Data de inscrição : 05/05/2020
Idade : 21
Localização : Rio de Janeiro-RJ
jopagliarin gosta desta mensagem
 Re: Equilíbrio Químico e Pressão
Re: Equilíbrio Químico e Pressão
Muito obrigada pela resposta e pela atenção Foconoita..... bom domingo para você!!! 




MiLory- Iniciante
- Mensagens : 9
Data de inscrição : 20/07/2020
Idade : 21
FocoNoIMEITA gosta desta mensagem
 Tópicos semelhantes
Tópicos semelhantes» Equilíbrio químico e pressão parcial
» Pressão Parcial e Equilíbrio Químico
» Equilíbrio Químico
» Equilíbrio químico - grau de equilíbrio
» Equilíbrio Químico
» Pressão Parcial e Equilíbrio Químico
» Equilíbrio Químico
» Equilíbrio químico - grau de equilíbrio
» Equilíbrio Químico
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













