UFC - termodinâmica
3 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 UFC - termodinâmica
UFC - termodinâmica
Oi, gente. Eu não entendi o gabarito dessa questão. Para mim seria a letra A a correta. Pois, como é uma isoterma, o ∆U seria zero, não? :scratch: Alguém poderia me explicar?
Obrigada desde já!
Obrigada desde já!
O "ciclo diesel", mostrado na figura abaixo, representa o comportamento aproximado de um motor diesel. A substância de trabalho desse motor pode ser considerada um gás ideal. O processo a-->b é uma compressão adiabática, o processo b-->c é uma expansão a pressão constante, o processo c-->d é uma expansão adiabática e o processo d-->a é resfriamento a volume constante.
Com relação a esses processos, assinale a opção correta.
a) No processo a -->b a energia interna do sistema não varia.
b) No processo b --> c a energia interna do sistema diminui.
c) No processo c--> d a energia interna do sistema diminui.
d) No processo d -->a a energia interna do sistema aumenta.
e) No ciclo completo a variação da energia interna é positiva.
- Spoiler:
- C

Liss Collins- Jedi

- Mensagens : 385
Data de inscrição : 30/09/2017
Idade : 24
Localização : BR
 Re: UFC - termodinâmica
Re: UFC - termodinâmica
Não são isotermas. A questão te diz que é uma compressão adiabática e expansão adiabática. A transformação adiabática é quando o gás não troca calor com o meio e isso não quer dizer que sua temperatura foi constante. Lembrando que os gráficos de uma isoterma e adiabáticas são parecidas.

RodrigoA.S- Elite Jedi

- Mensagens : 449
Data de inscrição : 12/07/2017
Idade : 24
Localização : Nova Iguaçu
 Re: UFC - termodinâmica
Re: UFC - termodinâmica
Oi, Rodrigo!
Caraca, verdade. Isso me passou batido mesmo
Então, deixo ver se eu entendi:
A letra A não seria, pois a energia interna do sistema varia, uma vez que o trabalho é positivo (sentido horário ali de a -->b), indício claro de que há variação de energia interna. No caso, há aumento da energia interna.
Estaria certo meu raciocínio?
Caraca, verdade. Isso me passou batido mesmo
Então, deixo ver se eu entendi:
A letra A não seria, pois a energia interna do sistema varia, uma vez que o trabalho é positivo (sentido horário ali de a -->b), indício claro de que há variação de energia interna. No caso, há aumento da energia interna.
Estaria certo meu raciocínio?

Liss Collins- Jedi

- Mensagens : 385
Data de inscrição : 30/09/2017
Idade : 24
Localização : BR
 Re: UFC - termodinâmica
Re: UFC - termodinâmica
Não, de c-->d a energia diminui. Veja essa imagem abaixo para te ajudar a entender melhor.
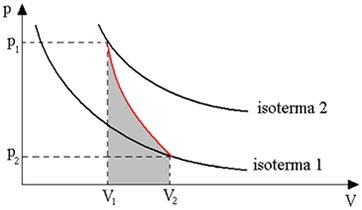
O gráfico da adiabática seria o vermelho. Perceba que ela vai de uma isoterma para outra, ou seja, tem variação de temperatura. Como T2>T1, se a transformação vai de T2 para T1, a energia diminui e do contrário, a energia aumenta.
OBS: No começo, eu quis responder a sua pergunta se de c-->d a energia iria aumentar, porém você editou e removeu.

O gráfico da adiabática seria o vermelho. Perceba que ela vai de uma isoterma para outra, ou seja, tem variação de temperatura. Como T2>T1, se a transformação vai de T2 para T1, a energia diminui e do contrário, a energia aumenta.
OBS: No começo, eu quis responder a sua pergunta se de c-->d a energia iria aumentar, porém você editou e removeu.

RodrigoA.S- Elite Jedi

- Mensagens : 449
Data de inscrição : 12/07/2017
Idade : 24
Localização : Nova Iguaçu
 Re: UFC - termodinâmica
Re: UFC - termodinâmica
Basta você lembrar daquela relação entre variação de energia interna com a variação da temperatura.Liss Collins escreveu:Oi, Rodrigo!
Caraca, verdade. Isso me passou batido mesmo
Então, deixo ver se eu entendi:
A letra A não seria, pois a energia interna do sistema varia, uma vez que o trabalho é positivo (sentido horário ali de a -->b), indício claro de que há variação de energia interna. No caso, há aumento da energia interna.
Estaria certo meu raciocínio?
∆U=3/2.n.R.∆T
Se a variação de temperatura for positiva ou negativa, a de energia também será,respectivamente.

RodrigoA.S- Elite Jedi

- Mensagens : 449
Data de inscrição : 12/07/2017
Idade : 24
Localização : Nova Iguaçu
 Re: UFC - termodinâmica
Re: UFC - termodinâmica
a - b é uma expansão adiabática (já que a questão diz), onde o volume é diminuído e pressão e temperatura aumentada. Se formos analisar a fórmula da variação de energia interna, vemos que:
φ = trabalho.
∆U = Q - φ
Como Q = m.c.T, se a T aumentar, consequentemente, o ∆U também vai aumentar.
Em c -d há uma compressão adiabática, situação contrária a anterior, volume aumentado e pressão e temperatura diminuida.
∆U = Q - φ
Como Q = m.c.T, se a T diminuir, consequentemente, o ∆U também vai diminuir.
c) está correta conforme minha análise.
PS: pessoal já respondeu muito bem aqui, mas para não ficar em vão o que eu digitei (já que colocaram enquanto digitava), vou deixar aqui para deixar ainda mais completo hahah.
φ = trabalho.
∆U = Q - φ
Como Q = m.c.T, se a T aumentar, consequentemente, o ∆U também vai aumentar.
Em c -d há uma compressão adiabática, situação contrária a anterior, volume aumentado e pressão e temperatura diminuida.
∆U = Q - φ
Como Q = m.c.T, se a T diminuir, consequentemente, o ∆U também vai diminuir.
c) está correta conforme minha análise.
PS: pessoal já respondeu muito bem aqui, mas para não ficar em vão o que eu digitei (já que colocaram enquanto digitava), vou deixar aqui para deixar ainda mais completo hahah.

Pedro29- Padawan

- Mensagens : 89
Data de inscrição : 15/02/2017
Idade : 27
Localização : Rio de Janeiro, RJ, Brasil
 Tópicos semelhantes
Tópicos semelhantes» Termodinâmica com MHS
» (EN) Termodinâmica
» Termodinamica
» 1ª Lei da Termodinâmica
» 1ª e 2ª Lei da Termodinâmica
» (EN) Termodinâmica
» Termodinamica
» 1ª Lei da Termodinâmica
» 1ª e 2ª Lei da Termodinâmica
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














