Termodinâmica UnB 2016
2 participantes
PiR2 :: Física :: Termologia
Página 1 de 1
 Termodinâmica UnB 2016
Termodinâmica UnB 2016
Considere as seguintes informações acerca do processo de explosão de um foguete de cores: as reações I e II ocorreram em sequência, com rendimento de 100%; a energia total liberada na explosão proveio exclusivamente da queima do enxofre presente na carga explosiva; o calor de combustão do enxofre nas condições termodinâmicas do processo foi igual a 310 kJ/mol; houve a decomposição de 207,9 g de perclorato de potássio. A partir dessas informações, calcule a energia total, em kJ, liberada na explosão do foguete. Após efetuar todos os cálculos solicitados, despreze, para a marcação no Caderno de Respostas, a parte fracionária do resultado final obtido, caso exista.
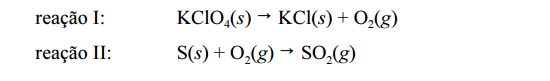
GABARITO : 930 KJ
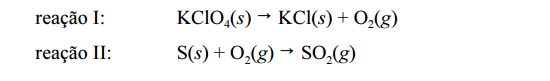
GABARITO : 930 KJ
karen__ ariely- Iniciante
- Mensagens : 44
Data de inscrição : 13/04/2016
Idade : 30
Localização : Brasília, Df, Brasil
 Re: Termodinâmica UnB 2016
Re: Termodinâmica UnB 2016
MM(KClO4) = 138.6 g/mol
207.9g de KClO4 equivalem a 1.5mol. Assim, pela proporção estequiométrica, será produzido 3 mols de O2.
Na reação II, temos que 1 mol de S reage com 1 mol de O2
Logo, teremos 3 mols de S
Assim, a energia liberada pelo enxofre vai ser 310*3 = 930KJ

CaiqueF- Monitor

- Mensagens : 1237
Data de inscrição : 16/05/2012
Idade : 28
Localização : Salvador -> São Carlos
 Re: Termodinâmica UnB 2016
Re: Termodinâmica UnB 2016
Caique F. , por quê eu não posso somar as reações pra obter a reação geral ? . Eu fiz isso, e a proporção deu :
1 mol de KCl pra 1 mol de S .
1 mol de KCl pra 1 mol de S .
karen__ ariely- Iniciante
- Mensagens : 44
Data de inscrição : 13/04/2016
Idade : 30
Localização : Brasília, Df, Brasil
 Re: Termodinâmica UnB 2016
Re: Termodinâmica UnB 2016
Você pode, desde que não esqueça de balancear a primeira equaçãokaren__ ariely escreveu:Caique F. , por quê eu não posso somar as reações pra obter a reação geral ? . Eu fiz isso, e a proporção deu :
1 mol de KCl pra 1 mol de S .

CaiqueF- Monitor

- Mensagens : 1237
Data de inscrição : 16/05/2012
Idade : 28
Localização : Salvador -> São Carlos
 Tópicos semelhantes
Tópicos semelhantes» Lei da termodinÂmica
» Termodinâmica
» (IFMS 2016) Termodinâmica
» UEM verão 2016 - Termodinâmica
» (IFPI 2016) História da termodinâmica
» Termodinâmica
» (IFMS 2016) Termodinâmica
» UEM verão 2016 - Termodinâmica
» (IFPI 2016) História da termodinâmica
PiR2 :: Física :: Termologia
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













