Solubilidade
3 participantes
Página 1 de 1
 Solubilidade
Solubilidade
(Fuvest) VALOR NUMÉRICO DO PRODUTO IÔNICO DA
ÁGUA=1,0×10-14
Leite de magnésia é essencialmente uma suspensão de
hidróxido de magnésio em água. A solubilidade de Mg(OH)‚, à
temperatura ambiente, é 1,5×10-4mol/L. Logo, o pH do leite de
magnésia está entre:
a)7 e 8
b)8 e 9
c)9 e 10
d)10 e 11
e)11 e 12
gabarito letra d
ÁGUA=1,0×10-14
Leite de magnésia é essencialmente uma suspensão de
hidróxido de magnésio em água. A solubilidade de Mg(OH)‚, à
temperatura ambiente, é 1,5×10-4mol/L. Logo, o pH do leite de
magnésia está entre:
a)7 e 8
b)8 e 9
c)9 e 10
d)10 e 11
e)11 e 12
gabarito letra d
Última edição por harrisonwow em Qua 21 Ago 2013, 00:10, editado 1 vez(es)
harrisonwow- Jedi

- Mensagens : 247
Data de inscrição : 09/05/2013
Idade : 30
Localização : Rio de Janeiro
 Re: Solubilidade
Re: Solubilidade
ta meio difícil de entender, procurei o enunciado na net, mas a resposta é minha então qualquer dúvida pode perguntar.
Mg(OH)2 ---> Mg^+2 + 2OH^-
1,5.10^-4 -------------2.1,5.10^4
[OH-] = 3.10^-4.
[H+].[OH-] = 10^-14 ==> [H+] = 10^-14/3.10^-4
[H+] = 10^-10/3
-log[H+] = pH ---> -log[10^-10/3] = pH
-pH = (log10^-10) - log3
-pH = -10 - (x < 1)
então letra d
obs: aquele x < 1 eu coloquei pra representar o log3 cujo o valor não passa de 1.
o valor dele exato é 0,477 se não me engano.
Mg(OH)2 ---> Mg^+2 + 2OH^-
1,5.10^-4 -------------2.1,5.10^4
[OH-] = 3.10^-4.
[H+].[OH-] = 10^-14 ==> [H+] = 10^-14/3.10^-4
[H+] = 10^-10/3
-log[H+] = pH ---> -log[10^-10/3] = pH
-pH = (log10^-10) - log3
-pH = -10 - (x < 1)
então letra d
obs: aquele x < 1 eu coloquei pra representar o log3 cujo o valor não passa de 1.
o valor dele exato é 0,477 se não me engano.
Última edição por Wilson Calvin em Qua 21 Ago 2013, 00:08, editado 1 vez(es)
Wilson Calvin- Matador

- Mensagens : 524
Data de inscrição : 26/02/2013
Idade : 26
Localização : São Paulo
 Re: Solubilidade
Re: Solubilidade
Edite o produto iônico da água, ficou uns simbolos ali no expoente. Vou dá um chute de que vale 10^{-14}.
Dissociação de hidróxido de magnésio:
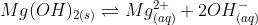
Se o símbolo (¥) que era pra ser 4 no produto iônico, pelo meu chute (mais provável), é o mesmo que está na solubilidade, que chutei 10^{-14}, então S deve ser 1,5.10^{-4} mol/L.
Sendo isso, é possível, por proporção estequiométrica, afirmar que:
[Mg{2+}] = 1,5.10^{-4} M / [OH-] = 3.10^{-4} M
Cálculos de pOH:
pOH = -log (3.10^{-4}) = -log 3 - log (10^{-4}) = - 0,477 + 4 = 3,523
Se o produto iônico é 10^{-14}:
pH + pOH = 14 --> pH = 14 - 3,523 = 10,477 --> Item D
Dissociação de hidróxido de magnésio:
Se o símbolo (¥) que era pra ser 4 no produto iônico, pelo meu chute (mais provável), é o mesmo que está na solubilidade, que chutei 10^{-14}, então S deve ser 1,5.10^{-4} mol/L.
Sendo isso, é possível, por proporção estequiométrica, afirmar que:
[Mg{2+}] = 1,5.10^{-4} M / [OH-] = 3.10^{-4} M
Cálculos de pOH:
pOH = -log (3.10^{-4}) = -log 3 - log (10^{-4}) = - 0,477 + 4 = 3,523
Se o produto iônico é 10^{-14}:
pH + pOH = 14 --> pH = 14 - 3,523 = 10,477 --> Item D

schow- Jedi

- Mensagens : 446
Data de inscrição : 03/01/2013
Idade : 28
Localização : Fortaleza-CE
 Re: Solubilidade
Re: Solubilidade
@editei ali, eu já tinha acertado, errei em operação básica. na soma de " - " com " - " 
Wilson Calvin- Matador

- Mensagens : 524
Data de inscrição : 26/02/2013
Idade : 26
Localização : São Paulo
 Re: Solubilidade
Re: Solubilidade
Desculpa consertei o erro ali em cima e que copiei a questao direto ai veio aqueles simbolos
harrisonwow- Jedi

- Mensagens : 247
Data de inscrição : 09/05/2013
Idade : 30
Localização : Rio de Janeiro
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













