ONNEQ-2008
2 participantes
Página 1 de 1
 ONNEQ-2008
ONNEQ-2008
Considere um ácido forte, hipotético, de fórmula H2B
a) Calcule o pH de uma solução de H2B de concentração 0,050 mol.L-1, admitindo a dissociação de um
único próton
b) Calcule o pH da mesma solução acima, admitindo que os dois prótons dissociam completamente
c) Experimentalmente foi determinado que o pH da solução citada acima era 1,27.
Com base nessa informação comente sobre a contribuição do ácido HB– para a acidez da solução.
d) Uma solução aquosa do sal NaHB apresentará pH maior, menor ou igual a 7 (sete)? Justifique
Agradeço desde já. Boa noite a todos !!
a) Calcule o pH de uma solução de H2B de concentração 0,050 mol.L-1, admitindo a dissociação de um
único próton
b) Calcule o pH da mesma solução acima, admitindo que os dois prótons dissociam completamente
c) Experimentalmente foi determinado que o pH da solução citada acima era 1,27.
Com base nessa informação comente sobre a contribuição do ácido HB– para a acidez da solução.
d) Uma solução aquosa do sal NaHB apresentará pH maior, menor ou igual a 7 (sete)? Justifique
Agradeço desde já. Boa noite a todos !!
Bruno Felipe- Iniciante
- Mensagens : 24
Data de inscrição : 22/01/2013
Idade : 26
Localização : Salvador
 Re: ONNEQ-2008
Re: ONNEQ-2008
A) Equação: 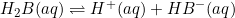
Se ∝ = 100%, por estequiometria:
[H2B] = [H+] = 0,050 M
pH = -log [H+] = - log (0,05) = 1,30
B) Equação :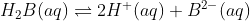
Se ∝ = 100%, por estequiometria:
[H+] = 2.[H2B] = 0,100 M
pH = -log [H+] = - log (0,1) = 1,00
C) Sendo um diácido forte, o H2B pode se ionizar e se dissociar conforme as reações:
Equação 1: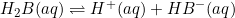 Ka(I)
Ka(I)
Equação 2: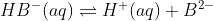 Ka(II)
Ka(II)
No item A, calculando-se o pH, para a primeira dissociação do ácido (equação 1), obteve-se um valor de 1,30. Considerando que ocorria dissociação completa dos dois prótons, no item B, obteve-se pH = 1,00. Se, experimentalmente, o pH encontrado foi de 1,27, conclui-se que a segunda dissociação (equação 2) teve uma contribuição mínima sobre o aumento da acidez da solução, ou seja, a segunda dissociação não foi completa. É possível afirmar que Ka(I) >>> Ka(II).
D) Apresentará pH maior que 7. O sal NaHB é formado por um cátion (Na+) de base forte (NaOH) e ânion (HB-) que, embora seja proveniente de um ácido forte, foi provado experimentalmente que tem um potencial baixo de sofrer dissociação (Ka(II) <<< Ka(I)). Desse modo, o ânion do sal citado sofre hidrólise, aumentando a basicidade do meio, conforme a reação:
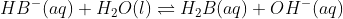
Trata-se, portanto, de um sal de caráter básico.
---
Espero que tenha ajudado.
Se ∝ = 100%, por estequiometria:
[H2B] = [H+] = 0,050 M
pH = -log [H+] = - log (0,05) = 1,30
B) Equação :
Se ∝ = 100%, por estequiometria:
[H+] = 2.[H2B] = 0,100 M
pH = -log [H+] = - log (0,1) = 1,00
C) Sendo um diácido forte, o H2B pode se ionizar e se dissociar conforme as reações:
Equação 1:
Equação 2:
No item A, calculando-se o pH, para a primeira dissociação do ácido (equação 1), obteve-se um valor de 1,30. Considerando que ocorria dissociação completa dos dois prótons, no item B, obteve-se pH = 1,00. Se, experimentalmente, o pH encontrado foi de 1,27, conclui-se que a segunda dissociação (equação 2) teve uma contribuição mínima sobre o aumento da acidez da solução, ou seja, a segunda dissociação não foi completa. É possível afirmar que Ka(I) >>> Ka(II).
D) Apresentará pH maior que 7. O sal NaHB é formado por um cátion (Na+) de base forte (NaOH) e ânion (HB-) que, embora seja proveniente de um ácido forte, foi provado experimentalmente que tem um potencial baixo de sofrer dissociação (Ka(II) <<< Ka(I)). Desse modo, o ânion do sal citado sofre hidrólise, aumentando a basicidade do meio, conforme a reação:
Trata-se, portanto, de um sal de caráter básico.
---
Espero que tenha ajudado.

schow- Jedi

- Mensagens : 446
Data de inscrição : 03/01/2013
Idade : 28
Localização : Fortaleza-CE
 Re: ONNEQ-2008
Re: ONNEQ-2008
Muito obrigado mais uma vez !!
Bruno Felipe- Iniciante
- Mensagens : 24
Data de inscrição : 22/01/2013
Idade : 26
Localização : Salvador
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













