(EEAR - 1988) Elétrons
3 participantes
Página 1 de 1
 (EEAR - 1988) Elétrons
(EEAR - 1988) Elétrons
O número máximo de elétrons num átomo que os apresenta distribuídos em cinco camadas é:
a) 54.
b) 58.
c) 92.
d) 106.
Editei o gabarito.
a) 54.
b) 58.
c) 92.
d) 106.
Editei o gabarito.
Última edição por ALDRIN em Qua 28 Out 2009, 19:03, editado 2 vez(es)

ALDRIN- Membro de Honra

- Mensagens : 950
Data de inscrição : 29/07/2009
Idade : 40
Localização : Brasília-DF
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
Olá Aldrin.
A eletrosfera do átomo está dividida em 7 regiões denominadas de níveis de energia ou camadas eletrônicas.
São as camadas K,L,M,N,O,P,Q,representadas pelos números 1,2,3,4,5,6,7 denominados de números quânticos principais e representados pela letra n.
O número máximo de elétrons em cada camada é calculado pela equação .
e=2n²
n=5
e=2*5²=2*25=50
O que aconteceu com o gabarito?
A eletrosfera do átomo está dividida em 7 regiões denominadas de níveis de energia ou camadas eletrônicas.
São as camadas K,L,M,N,O,P,Q,representadas pelos números 1,2,3,4,5,6,7 denominados de números quânticos principais e representados pela letra n.
O número máximo de elétrons em cada camada é calculado pela equação .
e=2n²
n=5
e=2*5²=2*25=50
O que aconteceu com o gabarito?
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
De acordo com a ordem do diagrama dá mais que 50.
K 1s²
L 2s² 2p6
M 3s² 3p6 3d10
N 4s² 4p6 4d10 4f14
O 5s² 5p6 5d10 5f14
P 6s² 6p6 6d10
Q 7s² 7p6 (somente em alguns livros)
A ordem do diagrama que se lê é:
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p6.
K 1s²
L 2s² 2p6
M 3s² 3p6 3d10
N 4s² 4p6 4d10 4f14
O 5s² 5p6 5d10 5f14
P 6s² 6p6 6d10
Q 7s² 7p6 (somente em alguns livros)
A ordem do diagrama que se lê é:
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p6.

ALDRIN- Membro de Honra

- Mensagens : 950
Data de inscrição : 29/07/2009
Idade : 40
Localização : Brasília-DF
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
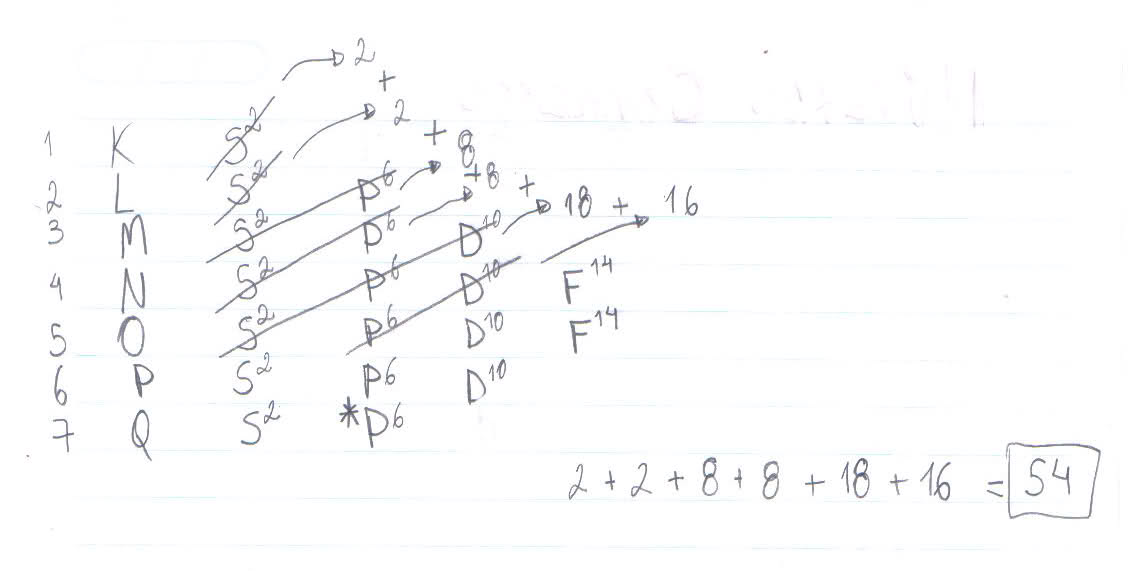
De acordo com o diagrama de Linus Pauling teremos:
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p6.
Para ser o que o gabarito diz temos que parar em 5p6,O que você acha?a quinta camada está no máximo de elétrons?
Se for acompanha "Nível de energia Camada Número máximo de elétrons" teremos:
K=2
L=8
M=18
N=32
O=32
T=92
E ai meu companheiro?
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p6.
Para ser o que o gabarito diz temos que parar em 5p6,O que você acha?a quinta camada está no máximo de elétrons?
Se for acompanha "Nível de energia Camada Número máximo de elétrons" teremos:
K=2
L=8
M=18
N=32
O=32
T=92
E ai meu companheiro?
kakaneves999@gmail.com gosta desta mensagem
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
Jeffson, a questão é trabalhosa e chata.
O que deu para entender é:
K 1s²
L 2s² 2p6
M 3s² 3p6 3d10
N 4s² 4p6 4d10
O 5s² 5p6
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6
2+2+6+2+6+2+10+6+2+10+6=54
O que deu para entender é:
K 1s²
L 2s² 2p6
M 3s² 3p6 3d10
N 4s² 4p6 4d10
O 5s² 5p6
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6
2+2+6+2+6+2+10+6+2+10+6=54

ALDRIN- Membro de Honra

- Mensagens : 950
Data de inscrição : 29/07/2009
Idade : 40
Localização : Brasília-DF
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
Olá Aldrin.
Então pelo jeito a unica explicação para ser isso é que depois de 5p6 irá vim o 6s² ou seja chegamos a sexta camada.
Então pelo jeito a unica explicação para ser isso é que depois de 5p6 irá vim o 6s² ou seja chegamos a sexta camada.
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
Sim, foi assim que pensei também.

ALDRIN- Membro de Honra

- Mensagens : 950
Data de inscrição : 29/07/2009
Idade : 40
Localização : Brasília-DF
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
Não sei se já encontraram a resposta, mas é o seguinte:
-
Existem dois tipos de distribuição:
Exemplo: Arsênio (As): Z = 33
Ordem energética (ordem de preenchimento): 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3
Ordem geométrica é a ordenação crescente de níveis energéticos, ou seja, pelas camadas.
Ordem geométrica (ordem de camada): 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p3
“Visualizando” a distribuição por ordem geométrica e usando as letras dos níveis (camadas), teremos as camadas energéticas: K = 2; L = 8; M = 18; N = 5
-

Existem dois tipos de distribuição:
Exemplo: Arsênio (As): Z = 33
Ordem energética (ordem de preenchimento): 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3
Ordem geométrica é a ordenação crescente de níveis energéticos, ou seja, pelas camadas.
Ordem geométrica (ordem de camada): 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p3
“Visualizando” a distribuição por ordem geométrica e usando as letras dos níveis (camadas), teremos as camadas energéticas: K = 2; L = 8; M = 18; N = 5
 Re: (EEAR - 1988) Elétrons
Re: (EEAR - 1988) Elétrons
Sim amigo Rafa.
Já encontramos pelo diagrama de Linus Pauling.
O raciocínio é de não chegar a camada superior a pedida ,ou seja,chegar até o máximo que nesse caso era o 5p6.
Forte abraço meu brother e agradecemos a sua participação .
Já encontramos pelo diagrama de Linus Pauling.
O raciocínio é de não chegar a camada superior a pedida ,ou seja,chegar até o máximo que nesse caso era o 5p6.
Forte abraço meu brother e agradecemos a sua participação .
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|














