Pressão exercida
2 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Pressão exercida
Pressão exercida
Bicarbonato de sódio, NaHCO3, é usado como fermento em bolos devido à decomposição do bicarbonato a altas temperaturas,
pela reação
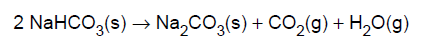
Os gases liberados na decomposição de 5,0 g de NaHCO3 foram recolhidos em um recipiente de 2,0 L, na temperatura de
27 °C. Considerando a constante universal dos gases 0,082 L.atm.K−1 . mol−1, a pressão exercida pelo CO2 (g) no recipiente
após completa decomposição do NaHCO3 foi de, aproximadamente,
(A) 0,15 atm.
(B) 0,37 atm.
(C) 0,73 atm.
(D) 1,5 atm.
(E) 3,7 atm.
Senhores, nessa questão eu tentei por p.v=n.r.t
No caso eu montei p.2 = 5.0,082.300
mas não esta batendo... acho que estou confundindo ao colocar os valores de acordo com a equação química...
uma ajuda por favor...
obrigada
pela reação
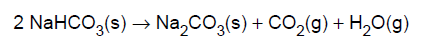
Os gases liberados na decomposição de 5,0 g de NaHCO3 foram recolhidos em um recipiente de 2,0 L, na temperatura de
27 °C. Considerando a constante universal dos gases 0,082 L.atm.K−1 . mol−1, a pressão exercida pelo CO2 (g) no recipiente
após completa decomposição do NaHCO3 foi de, aproximadamente,
(A) 0,15 atm.
(B) 0,37 atm.
(C) 0,73 atm.
(D) 1,5 atm.
(E) 3,7 atm.
- Resposta:
- B
Senhores, nessa questão eu tentei por p.v=n.r.t
No caso eu montei p.2 = 5.0,082.300
mas não esta batendo... acho que estou confundindo ao colocar os valores de acordo com a equação química...
uma ajuda por favor...
obrigada

ccclarat- Recebeu o sabre de luz

- Mensagens : 107
Data de inscrição : 30/08/2018
Idade : 31
Localização : Sao Paulo, Sao Paulo
 Re: Pressão exercida
Re: Pressão exercida
Você está colocando n = 5 , mas está considerando 5 mols = 5g ?
2 mol NaHCO3( Equivale a 168g) -- CO2 (Equivale a 44g)
x mol NaHCO3(Equivalerá a 5g ) -- Y gramas de CO2.
5*44/168 = Y --> Y ≈ 1,30g, como quer saber a pressão de CO2 --> PV=NRT --> 2P = (1,30*0,082*300)/44 --> 2P = 0,726 --> P ≈ 0.37
** Fiz algumas aproximações,como já foi feita no início, o erro se propaga até o final mas não altera o gabarito aí.
2 mol NaHCO3( Equivale a 168g) -- CO2 (Equivale a 44g)
x mol NaHCO3(Equivalerá a 5g ) -- Y gramas de CO2.
5*44/168 = Y --> Y ≈ 1,30g, como quer saber a pressão de CO2 --> PV=NRT --> 2P = (1,30*0,082*300)/44 --> 2P = 0,726 --> P ≈ 0.37
** Fiz algumas aproximações,como já foi feita no início, o erro se propaga até o final mas não altera o gabarito aí.
Kayo Emanuel Salvino- Fera

- Mensagens : 588
Data de inscrição : 21/05/2017
Idade : 21
Localização : João Pessoa, Paraíba e Brasil.
 Re: Pressão exercida
Re: Pressão exercida
kayo, obrigada pela ajuda!!!
fiquei com uma duvida
2P = (1,30*0,082*300)/44 --- o 44... pq dividir por ele? o n nao seria 1,30? ou e a massa molar?
fiquei com uma duvida
2P = (1,30*0,082*300)/44 --- o 44... pq dividir por ele? o n nao seria 1,30? ou e a massa molar?

ccclarat- Recebeu o sabre de luz

- Mensagens : 107
Data de inscrição : 30/08/2018
Idade : 31
Localização : Sao Paulo, Sao Paulo
 Tópicos semelhantes
Tópicos semelhantes» Pressão exercida por um gás perfeito
» A pressão exercida por 12 g de um gás ideal n
» Pressão exercida ( Hidrostática)
» Pressão exercida por um gás, propondo que ele
» Calculo da pressao exercida no solo
» A pressão exercida por 12 g de um gás ideal n
» Pressão exercida ( Hidrostática)
» Pressão exercida por um gás, propondo que ele
» Calculo da pressao exercida no solo
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













