Balanceameto por oxi-redução
3 participantes
PiR2 :: Química :: Físico-Química
Página 1 de 1
 Balanceameto por oxi-redução
Balanceameto por oxi-redução
Aman)Ajuste a equação por oxi-redução,os coeficientes da reação :
H2SO4 + Cu -----> CuSO4 + SO2 + H2O
Se você somar os coeficientes encontrados obeterá o seguinte valor
A)10
B)9
C)6
D)7
E)8
Eu acho que estou errando o numero de oxidação do cobre no CuSO4,Poderiam me ajudar por favor
Gabarito letra D
H2SO4 + Cu -----> CuSO4 + SO2 + H2O
Se você somar os coeficientes encontrados obeterá o seguinte valor
A)10
B)9
C)6
D)7
E)8
Eu acho que estou errando o numero de oxidação do cobre no CuSO4,Poderiam me ajudar por favor
Gabarito letra D

jonathas.jbr- Padawan

- Mensagens : 97
Data de inscrição : 12/05/2016
Idade : 26
Localização : Rio de Janeiro
 Re: Balanceameto por oxi-redução
Re: Balanceameto por oxi-redução
nox de Cu é +2 por a carga iônica do sulfato é 2-. Com esse valor, você calcula os coeficientes:
2H2SO4 + Cu -> CuSO4 + SO2 + 2H2O
Soma dos coeficientes: 7
Método eficiente para balanceamento por oxi-redução:
https://pir2.forumeiros.com/t104259-oxirreducao
Abraço!
Se não conseguir, posto a solução.
2H2SO4 + Cu -> CuSO4 + SO2 + 2H2O
Soma dos coeficientes: 7
Método eficiente para balanceamento por oxi-redução:
https://pir2.forumeiros.com/t104259-oxirreducao
Abraço!
Se não conseguir, posto a solução.

gabrieldpb- Fera

- Mensagens : 284
Data de inscrição : 08/02/2016
Idade : 29
Localização : Ribeirão Preto
 Re: Balanceameto por oxi-redução
Re: Balanceameto por oxi-redução
gabrieldpb, posta a solução, por favor. Depois de achar a variação do Nox do Cu e do S e vou balancear, o do S interfere, pois temos 2 no produto. Se puder um passo a passo, agradeceria.

Gustavoadp- Estrela Dourada

- Mensagens : 1036
Data de inscrição : 05/07/2014
Idade : 26
Localização : Recife, PE
 Re: Balanceameto por oxi-redução
Re: Balanceameto por oxi-redução
Olhe a estrutura do CuSO4:
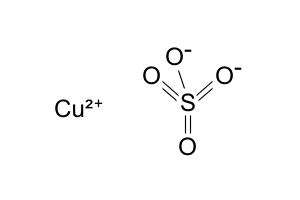
Cada O tem nox -2, como tem 4 o nox total de todos os O's é -8. Para completar a carga iônica 2- do ânion sulfato, S tem nox +6. O Cu tem nox +2, pois doou dois e- para o ânion.
Dado isso, vamos ao método de balanceamento ao qual me referi. Veja na equação química, que Cu foi oxidado (0 -> +2) e o enxofre foi reduzido (+6 -> +4).
Então, as minhas semi-reações são:
Cu -> Cu(2+) oxidação
SO4(2-) -> SO4(2-) + SO2 redução
Vamos balancear todos os termos que não sejam H ou O:
Cu -> Cu(2+)
2SO4(2-) -> SO4(2-) + SO2
Vamos balancear O com H2O:
Cu -> Cu(2+)
2SO4(2-) -> SO4(2-) + SO2 + 2H2O
Como estamos em solução ácida, balanceie o H com H+:
Cu -> Cu(2+)
2SO4(2-) + 4H(+) -> SO2 + 2H2O
Vamos balancear as cargas elétricas adicionando e-:
Cu -> Cu(2+) + 2e-
2SO4(2-) + 4H(+) + 2e- -> SO2 + 2H2O
Multiplicar cada equação por um fato que deixe um número igual de elétrons, para que quando a somá-las, os e- desapareçam. Nesse caso, deixamo-as como estão, pois ao somá-las os e- já terão sumido:
4H(+) + 2SO4(2-) + Cu -> Cu(2+) + SO4(2-) + SO2 + 2H2O
Mas o que seria 4H(+) + 2SO4(2-)?
2 H2SO4
2 H2SO4 + Cu -> CuSO4 + SO2 + 2H2O
Espero que tenha entendido. Abraço!

Cada O tem nox -2, como tem 4 o nox total de todos os O's é -8. Para completar a carga iônica 2- do ânion sulfato, S tem nox +6. O Cu tem nox +2, pois doou dois e- para o ânion.
Dado isso, vamos ao método de balanceamento ao qual me referi. Veja na equação química, que Cu foi oxidado (0 -> +2) e o enxofre foi reduzido (+6 -> +4).
Então, as minhas semi-reações são:
Cu -> Cu(2+) oxidação
SO4(2-) -> SO4(2-) + SO2 redução
Vamos balancear todos os termos que não sejam H ou O:
Cu -> Cu(2+)
2SO4(2-) -> SO4(2-) + SO2
Vamos balancear O com H2O:
Cu -> Cu(2+)
2SO4(2-) -> SO4(2-) + SO2 + 2H2O
Como estamos em solução ácida, balanceie o H com H+:
Cu -> Cu(2+)
2SO4(2-) + 4H(+) -> SO2 + 2H2O
Vamos balancear as cargas elétricas adicionando e-:
Cu -> Cu(2+) + 2e-
2SO4(2-) + 4H(+) + 2e- -> SO2 + 2H2O
Multiplicar cada equação por um fato que deixe um número igual de elétrons, para que quando a somá-las, os e- desapareçam. Nesse caso, deixamo-as como estão, pois ao somá-las os e- já terão sumido:
4H(+) + 2SO4(2-) + Cu -> Cu(2+) + SO4(2-) + SO2 + 2H2O
Mas o que seria 4H(+) + 2SO4(2-)?
2 H2SO4
2 H2SO4 + Cu -> CuSO4 + SO2 + 2H2O
Espero que tenha entendido. Abraço!

gabrieldpb- Fera

- Mensagens : 284
Data de inscrição : 08/02/2016
Idade : 29
Localização : Ribeirão Preto
 Re: Balanceameto por oxi-redução
Re: Balanceameto por oxi-redução
Obrigado ajudou muito Gabriel !

jonathas.jbr- Padawan

- Mensagens : 97
Data de inscrição : 12/05/2016
Idade : 26
Localização : Rio de Janeiro
PiR2 :: Química :: Físico-Química
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













